

CRISPR-U™是源井生物自主研发的基因编辑技术(基于CRISPR / Cas9技术),CRISPR-U™技术比普通CRISPR/Cas9技术的基因切割效率更高,同时可以大幅度提升同源重组效率,轻松实现细胞和动物水平的基因敲除(KO)、基因点突变(PM)和基因敲入(KI)。利用CRISPR-U™的技术优势,源井生物已成功在超过100种细胞系上实现基因编辑。
CRISPR/Cas9系统的原理是利用gRNA特异性识别靶序列,并引导Cas9核酸内切酶对靶序列的PAM上游进行切割,从而造成靶位点DNA双链断裂,随之利用细胞的非同源末端连接(NHEJ)或同源重组(HDR)的方式对切割位点进行修复,实现DNA水平的敲除、敲入或点突变。
· 技术优势 ·

· 基因敲除细胞系 ·
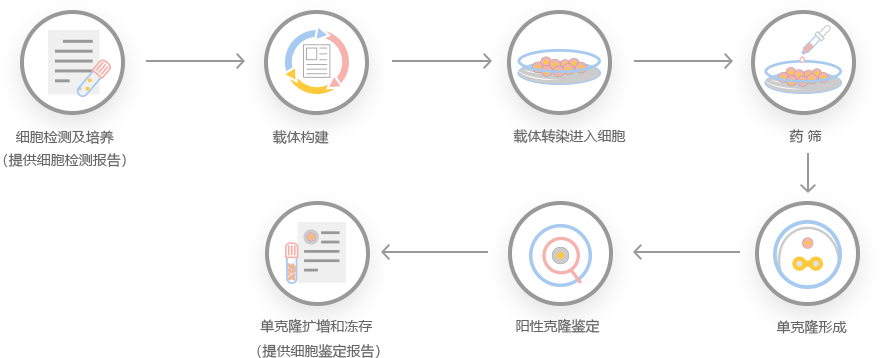
单克隆培养。选择不同的克隆分别进行靶位点扩增及测序验证,筛选出基因敲除的阳性克隆。
·常见基因敲除细胞系类型

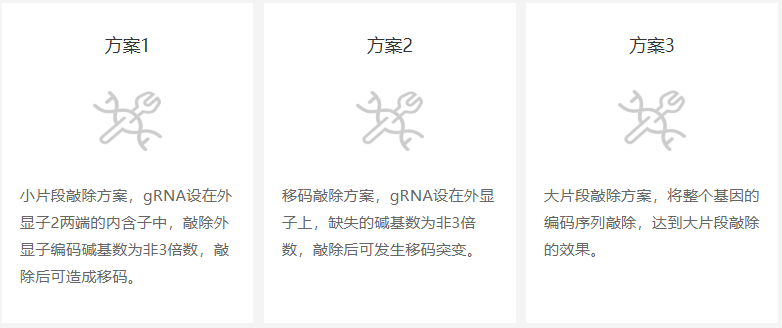
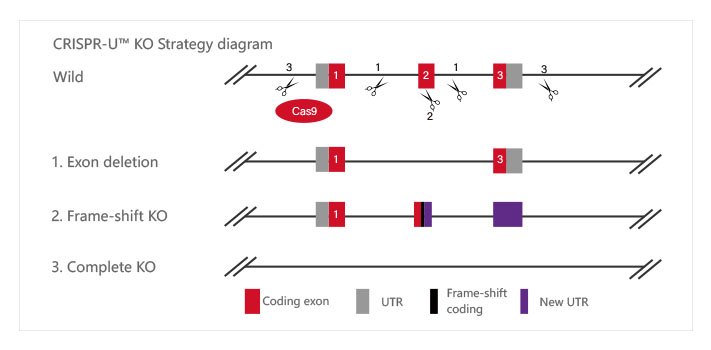
· 敲除方案 ·
源井生物根据客户需求,结合靶基因的情况进行敲除方案设计。
· 服务流程及质量控制 ·
· 应用案例 ·
中国仓鼠卵巢(CHO)细胞被用作生物工厂,用于生产一系列重组治疗蛋白,包括单克隆抗体和Fc融合蛋白。宿主细胞蛋白(HCP)是必须从治疗制剂中去除的杂质,因为它们具有潜在的免疫原性风险。虽然在典型的下游净化过程中,大多数HCP杂质被有效去除,但清除少量存在的HCP仍然是一个挑战。利用CRISPR/Cas9系统建立Anxa2和Ctsd基因敲除CHO细胞系,并证实了细胞裂解液中HCP完全消除。在培养过程中,所有的敲除细胞系都显示出与野生型对照相似的生长和活力。因此,敲除非必需基因可以减少重组治疗蛋白生产中HCP的污染。
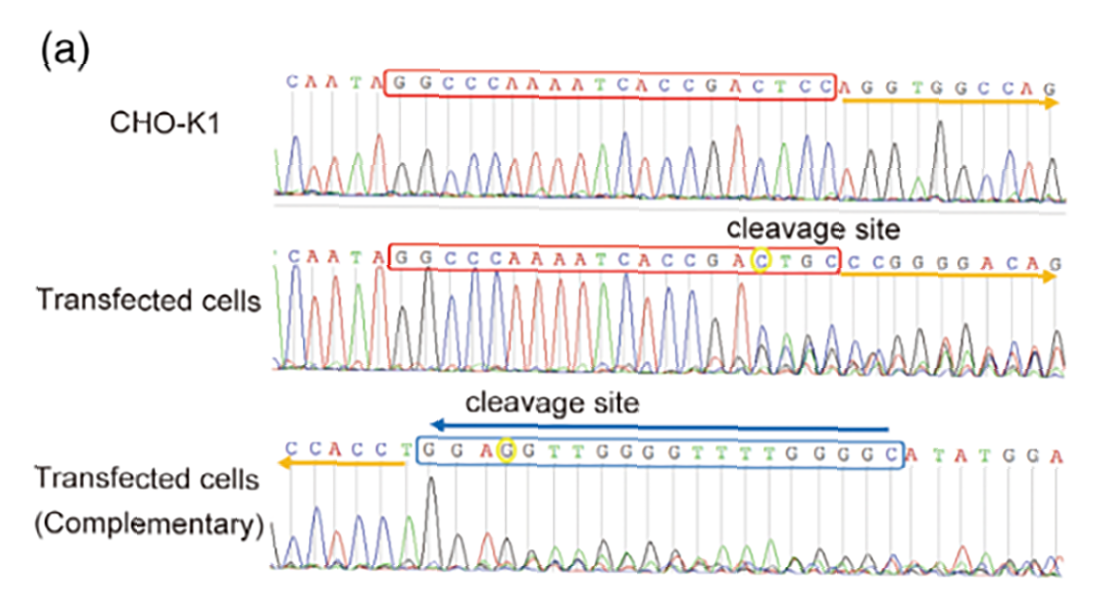
(a)sgRNA打靶Anxa2基因的4号外显子。
对序列进行双向分析。
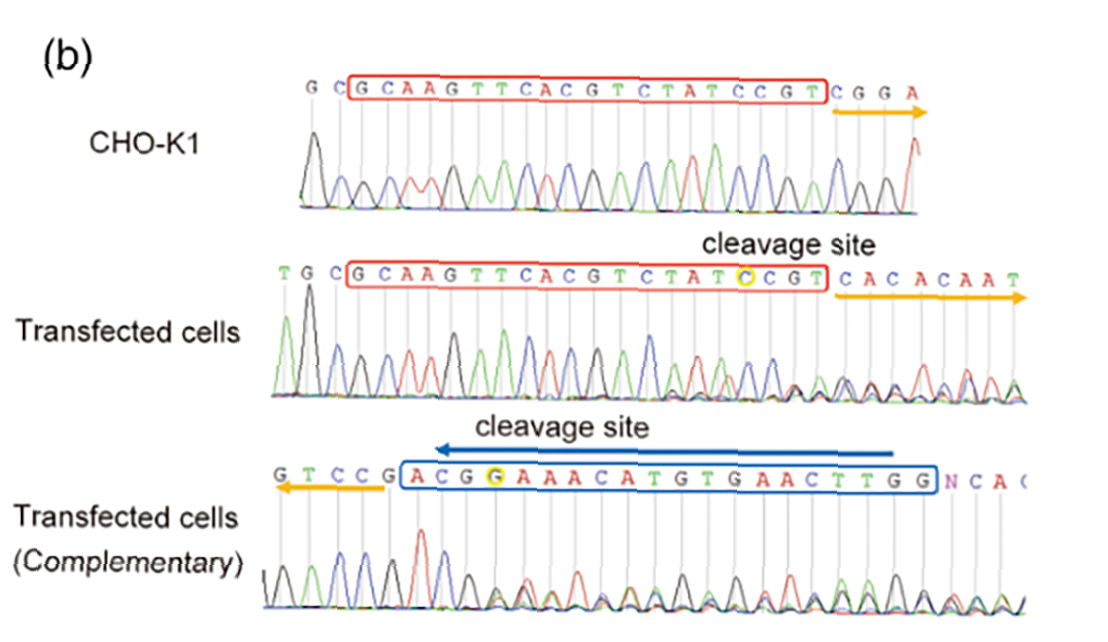
(b) sgRNA打靶Ctsd基因2号外显子。
对序列进行双向分析。
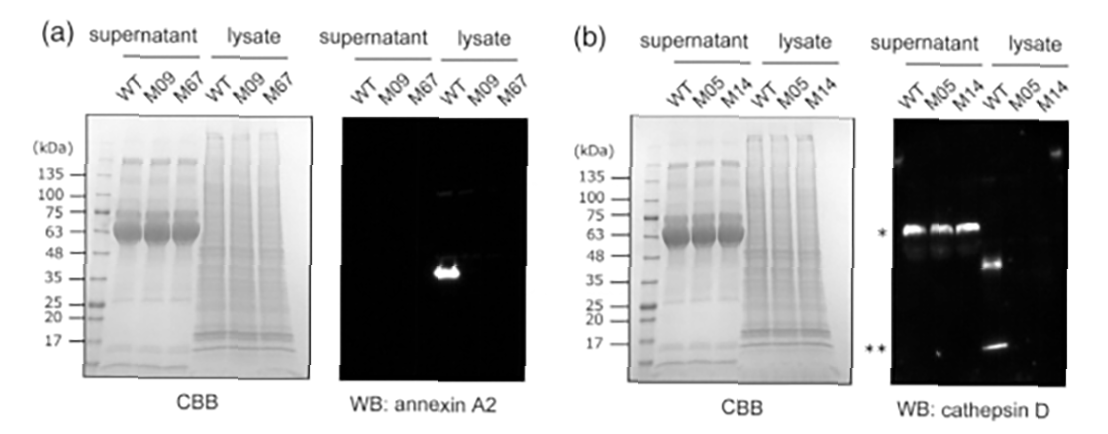
用SDS-PAGE和WB分析鉴定CHO基因敲除细胞株的蛋白表达。
(a) Anxa2基因敲除细胞系。
(b) Ctsd敲除细胞系。细胞培养上清液(47μg蛋白)和细胞裂解液(20μg蛋白)经4-20%SDS-PAGE分析。
CBB染色检测总蛋白。利用各自的捕获和检测抗体对每个蛋白质进行WB分析。星号表示非特定波段。双星号表示组织蛋白酶D的片段
在蛋白质表达分析中,没有观察到CHO-K1(WT)细胞系中的细胞培养上清液中的膜联蛋白A2和组织蛋白酶D。对贴壁的CHO-K1细胞进行静态培养,在培养过程中没有物理应力诱导细胞裂解,这表明CHO细胞分泌的这些蛋白质数量相当少。此外,在对Anxa2和Ctsd基因敲除细胞系的蛋白质表达分析中,没有观察到任何截短的HCP。
Reference:
Fukuda, N., Senga, Y., & Honda, S. (2019). Anxa2‐and Ctsd‐knockout CHO cell lines to diminish the risk of contamination with host cell proteins. Biotechnology progress, e2820.
原文阅读:https://www.ubigene.com/service/cell/15.html







评论