1】常规慢病毒,由于
-
T细胞膜上受体的不稳定;
-
非激活的T细胞本身无增殖能力;
-
T细胞内部有阻碍反转录的机制等原因而导致慢病毒的T细胞感染能力 偏弱,需要多次重复感染,且对于实验操作的条件要求十分苛刻
2】体外培养的T细胞本身十分敏感且脆弱,慢病毒感染对细胞的状态影响非常大 3】T细胞是悬浮细胞,进一步加大了感染的难度
遇上这样“磨人的细胞”怎么办?

汉恒病毒载体工程师们深切体会到了大家的痛苦
通过多次实验,研发出适用于原代T细胞基因操作的悬浮细胞专用的腺病毒(Ads)和慢病毒(hTLv)。其中Ads也非常适用感染其他悬浮细胞,如Jurkat,K562,HL-60和L1210等。慢病毒hTLv适用人原代T细胞的感染还可以用来构建稳转系。
汉恒病毒感染效果图
汉恒原代T细胞感染实例——使用悬浮细胞专用腺病毒ads感染
悬浮细胞专用腺病毒Ads感染小鼠原代CD4+ T细胞
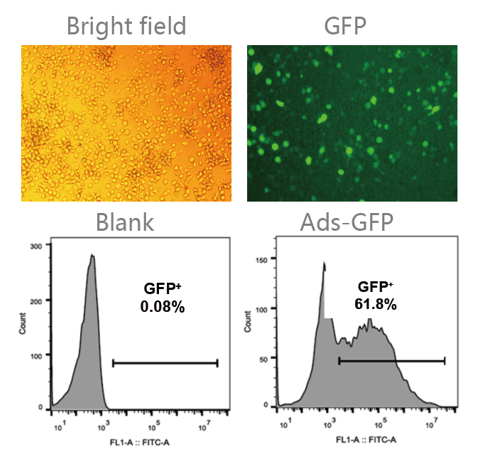
细胞:小鼠原代CD4+ T细胞
刺激方式:CD3/CD28抗体和IL-2激活48h
病毒:Ads-GFP, 1×10^10 PFU/ml
使用方式:MOI=500
悬浮细胞专用腺病毒Ads感染人原代CD4+ T细胞
细胞:人原代CD4+ T细胞
刺激方式:CD3/CD28抗体和IL-2激活48h
病毒:Ads-GFP, 1×10^10 PFU/ml
使用方式:MOI=100
汉恒原代T细胞感染实例——使用慢病毒
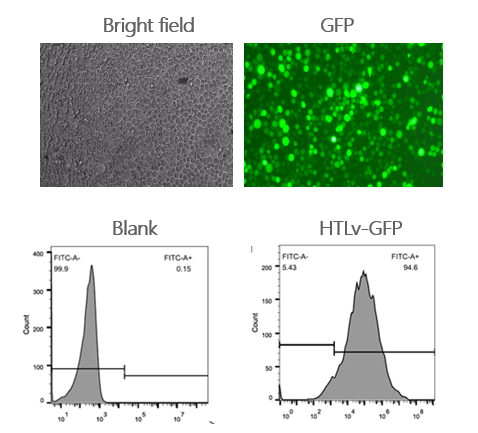
原代T细胞专用病毒-慢病毒感染人原代CD4+ T细胞

细胞:人原代CD4+ T细胞
刺激方式:CD3/CD28抗体和IL-2激活48h
病毒:hTLv-GFP,1*10^8 TU/ml
使用方式:MOI=50
上文我们了解到T细胞是很难被感染的,除了使用正确的病毒工具外,在细胞制备后想要成功感染T细胞还有两个关键步骤:细胞体外刺激、细胞感染
细胞体外刺激
1. 按照小鼠或人源 CD4+T 细胞分离 kit (Thermo) 说明书分离得到 CD4+T 细胞。 2. 取所需体积的 PBS,按照 5 μg/ml 的终浓度加入 Anti-mouse CD3e 和 Anti-mouse CD28 抗体,500 μl/孔包被 Non-Treated 24-well plate,室温放置 4 h,吸掉抗体悬液,加入 500 μl 1% BSA(PBS 配置)室温封闭 30 min,封闭结束加入 500 μl PBS 洗孔一次。 注:请在分离细胞的同时准备好平板,包括后续感染所需的量。
3.将分离得到的 CD4+ T 按照浓度 5x105 cell/ml 重悬在完全 T 细胞培养基中(1640,10% FBS,1% penicillin-streptomycin, 50 μM β-mercaptoethanol, 100 U/ml IL-2),将细胞加入步骤 2 中包被处理好的平板,2 ml 每孔(1x106 cell/well),然后放入 37℃ CO2培养箱刺激培养 48 h。细胞在刺激 24 h 后体积略微增大,进入活化状态,刺激 48 h 后可进行病毒感染。
细胞感染
1. 收集活化好的 CD4+T 细胞,400 g 离心 5 min。用 T 细胞培养基重悬计数备用,在收集的过程中发现有些细胞会贴壁,此为正常现象,可反复吹打至贴壁的细胞也呈悬浮状态。
注:具体 MOI 选择可在 96 孔板中预实验进行梯度摸索,对于慢病毒建议使用 10,30,100 的梯度进行,对于腺病毒建议使用 500,1000,1500 的梯度进行摸索。
注:离心结束观察细胞分散状态,除非细胞全聚集在一处,否则不建议吹散细胞。
4. 感染结束后取出培养板,小心吸掉感染孔中 350 μl 的培养基(70%),加入 1.85 ml 的 T 细胞完全培养基补足体积为 2 ml 并吹打混匀。
5. 可选步骤:病毒感染 24 h 后,小心吸掉培养基,在同一培养皿中按照 2-4 步进行病毒复感染操作。
注:感染后刺激的细胞增殖较快,请注意观察细胞密度并使其维持在 1x106/ml 左右。此外,如果需要让细胞增殖较长时间,为了防止其过度活化,可撤掉抗体的刺激。


评论