发育生物学的核心问题是多细胞生物体如何从单细胞受精卵发育而来。探索发育过程中究竟有多少种细胞类型以及不同细胞命运是如何产生的是发育生物学的重要目标。
常规质控
a. 细胞数目、数据量、基因数量
b. 细胞类型:聚类是否受批次、细胞周期、测序深度等影响
c. 细胞类型:注释出的类型是否符合预期
d. 基因表达:差异表达基因 (DEGs) 的数目、DEGs 的 GO、KEGG 等功能分析
e. 基因表达:各细胞类型已知标记基因 (marker) 的检出情况
分析角度
f. 新的细胞类型 novel cell type
g. 新的基因表达 novel cell type marker
h. 推测细胞类型的空间位置 spatial location
i. 细胞类型占比、占比构成随时间的变化 (涉及不同时期数据时)
j. 细胞谱系构建 cell fate trajectories
k. 细胞互作 cell-cell interaction
l. 类型分化的基因表达变化
m. 不同时期、来源的数据整合 data integration
n. 跨物种比较 cross-species comparison
分析策略
新的细胞类型及新的基因表达
对细胞类型和基因表达的刻画是单细胞测序文章分析的第一步。如果能够发现发育、疾病等进程中前人未报导的新细胞类型或新基因表达,往往能给文章增色不少,也通常能启发下游的分析思路。这一步需要较多的文献知识积累,包括所测样本的细胞类型及标记基因信息。
在发现新类型上,可以是之前从未报道的细胞类型;也可以是,某体系中不预期存在的细胞类型,但这种细胞类型本身可以不是新的。比如,Caoet al., Science2020 在脾中发现了 hepatoblast-like 细胞,在肾上腺中发现了 trophoblast-like 细胞 [1]。这两种细胞并非新类型,但却未在脾和肾上腺报导过。在发现新基因表达上,可以关注某种细胞类型表达的除该类型已知功能相关基因外的、其它的功能基因的富集;也可以关注中间状态细胞类型的基因共表达情况。如 Donget al., Genome Biology 2018 关注了一个重要过程 —— 上皮和间充质的互相转变:EMT& MET,并研究了此过程涉及的细胞类型的基因表达,发现了在上皮细胞中间充质基因的共表达 [2]。
推测细胞类型的空间位置
在发育中,细胞沿前后轴、背腹轴等体轴进行发育,形成不同的组织器官、细胞类型。比如,在内胚层发育中,咽、肝、肺、胃、胰岛等器官沿前后轴在不同位置发育。那么,这些空间位置信息是否反映在单细胞转录组层面呢?针对有不同位置来源(尤其是有前后轴分布差异)的样本时,可以对细胞构建拟空间轴,并利用 Hox 簇的表达进行比较验证,探索单细胞转录组中的空间位置信息。
数据整合和跨物种比较
目前已经发表了多种物种、多个时期的单细胞转录组数据,这些数据提供了丰富的细胞构成和基因表达信息。一方面,结合自己的数据集和已发表的数据进行跨物种比较,是研究进化上物种间细胞类型构成相似度、同源类型基因表达保守性的有效手段。另一方面,同一物种同一发育系统内前后时期的数据整合,让我们可以在更大的时间跨度更全面地探索细胞分化发育路径。在设计文章时,可以考虑整合已发表的数据和自己的数据进行分析。一般情况下,整合分析需尽量选择相同平台、相同实验方法来源的数据集。不同的实验平台(如 Smart-seq2vs 10X Genomics)、不同的实验方法(细胞测序 vs 核测序)有较高的整合难度,并且整合分析所得结论的可靠性也会打折扣。
文章设计
图表安排
图 1. 描述采样信息并展示细胞聚类及类型注释结果
Fig1. Identification and characterization ofcell types
图 2. 发现了新的细胞类型或新的类型特异表达,并通过实验验证了新类型或新基因表达
Fig2. Novel cell type(s) / novel geneexpression, experimental validation of novel finding
图 3. 全局性的「关注」基因的表达特征(如信号分子à细胞互作、转录因子等)
Fig3. Expression patterns of particular genesets (signalingàcell-cell interaction, TF)
图 4. 选取感兴趣的发育体系,进行发育路径构建,并描述发育路径下的驱动基因
Fig4. Characterization of developmentaltrajectories (of specific organs/tissues/cases)
图 5. 数据整合(如跨物种比较;结合更早 / 晚的数据进行分析)
Fig5. Data integration (cross-speciescomparison; data integration with early/late stages)
图 1. 展示采样信息、细胞聚类结果,并刻画类型占比变化
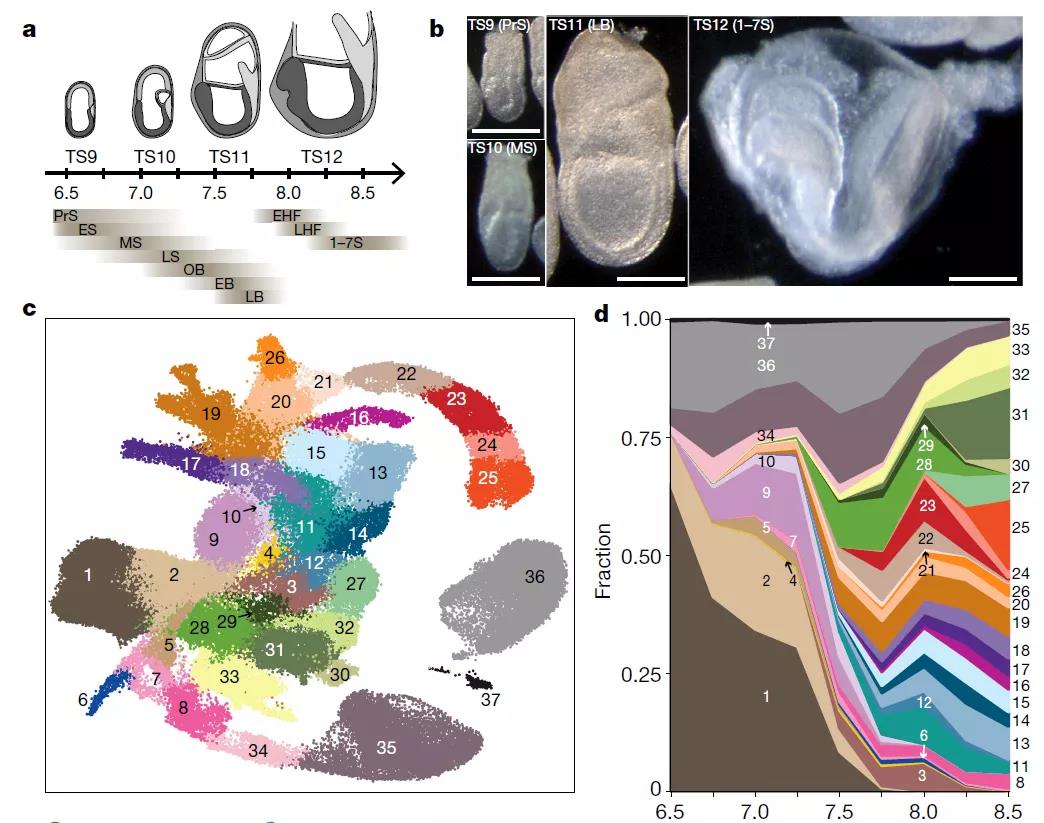
(Pijuan-Salaet. al., Nature, 2019; Figure 1)
图 2. 发现了新的细胞类型或新的类型特异表达,并通过实验验证了新类型或新基因表达
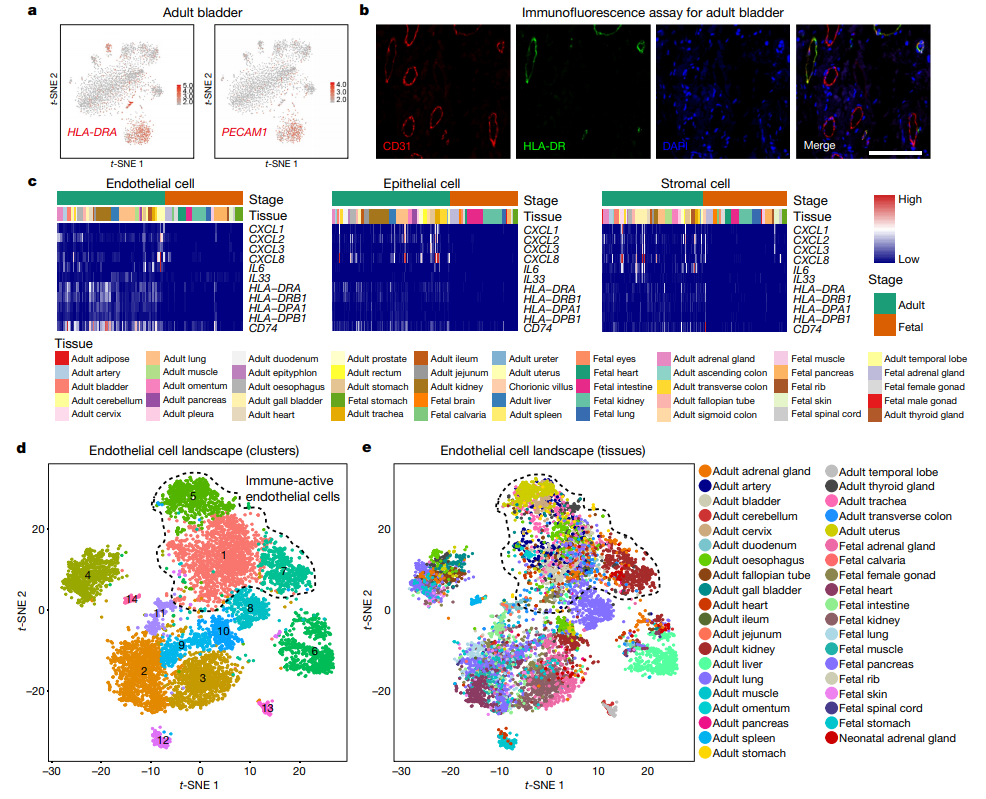
(Hanet. al., Nature, 2020; Figure 2)
图 3. 通过不同信号通路受体配体的表达研究细胞互作
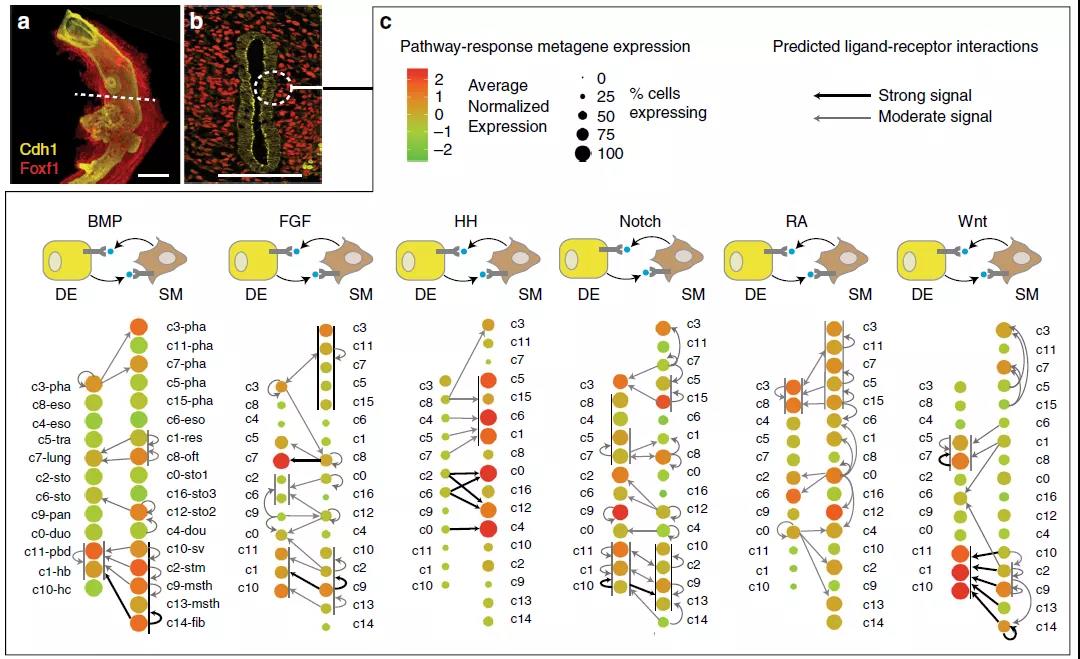
(Hanet. al., Nature communications, 2020)
图 4. 细胞类型间的谱系信息

(Sladitscheket. al., Cell, 2020; Figure 3)
图 5. 数据整合 —— 跨物种比较
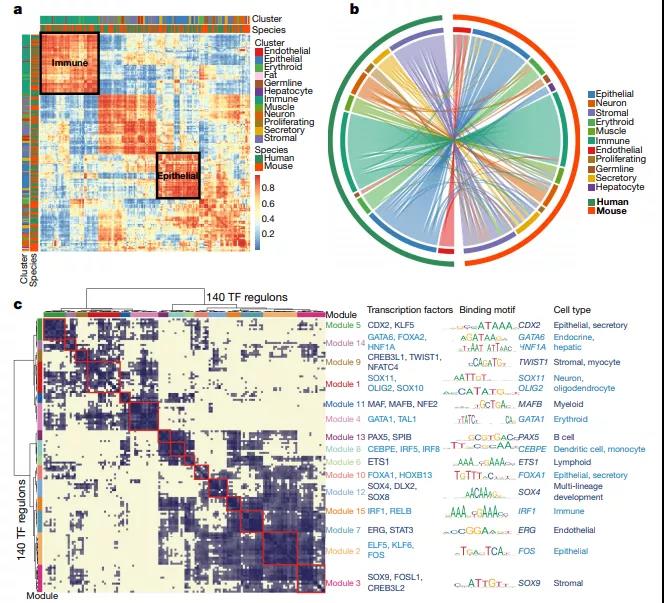
(Hanet. al., Nature, 2020; Figure 2)
以上就是我们为大家整理的应用单细胞测序到发育生物学的文章整体分析思路以及文章设计框架,希望对大家有所帮助。
一步了解单细胞多组学技术和应用实例,以及提高其相关测序数据分析的能力和技巧。西安交通大学基础医学院联合陕西省科学技术协会特邀请多位国内单细胞测序领域的专家学者,于 2021 年 9 月在陕西省西安市举办「单细胞多组学技术与生物信息学分析研习班」。
联系方式
联系人:张老师;
电话:18016021036;
邮箱:zhangziyi@genenergy.cn
客服微信:genenergy
参考文献:
[1] JCao, O'Day D R, Pliner H A, et al. A human cell atlas of fetal geneexpression[J]. Science, 370.
[2] DongJ, Hu Y, Fan X, et al. Single-cell RNA-seq analysis unveils aprevalent epithelial/mesenchymal hybrid state during mouseorganogenesis[J]. Genome Biology, 2018, 19(1):31.
[3] BlancaP S, Griffiths J A, Carolina G, et al. A single-cell molecular map ofmouse gastrulation and early organogenesis[J]. Nature, 2019,566(7745):490-495.
[4]X Han, Zhou Z, Fei L, et al. Construction of a human cell landscapeat single-cell level[J]. Nature, 2020, 581(7808).
[5] HanL, Chaturvedi P, Kishimoto K, et al. Single cell transcriptomicsidentifies a signaling network coordinating endoderm and mesodermdiversification during foregut organogenesis[J]. NatureCommunications, 2020.
[6] SladitschekH L, Fiuza U M, Pavlinic D, et al. MorphoSeq: Full Single-CellTranscriptome Dynamics Up to Gastrulation in a Chordate[J]. Cell,2020, 181(4).









评论