前言
2021 年 1 月 5 日,浙江大学孙红祥教授作为通讯作者,在 Cell Reports (IF: 8.109) 发表了题为“linc-AAM Facilitates Gene Expression Contributing to Macrophage Activation and Adaptive Immune Responses”的研究论文,报道了 lncRNA linc-AAM 作为转录增强子激活巨噬细胞并促进适应性免疫的分子机制。

文章中表达谱芯片实验和分析由欧易生物协助完成。
研究背景
巨噬细胞作为重要的先天性免疫细胞,可以在链接先天性免疫和获得性免疫之间发挥重要作用。lncRNA 作为一类重要的非编码 RNA,参与了不同的生物学过程中对 mRNA 表达的调控。但目前已报道的参与免疫细胞活化的 lncRNA 较少,尤其是参与调节适应性免疫反应的 lncRNA 鲜见报道。本研究重点探讨 lncRNA 参与巨噬细胞活化的分子机制,并采用基因敲除小鼠研究 lncRNA 对适应性免疫应答的调控作用。
研究内容
本研究发现与鉴定了一个与巨噬细胞活化相关的 lncRNA linc-AAM,并对其功能和机制进行了详细研究。linc-AAM 在活化的巨噬细胞中高表达;分别对 linc-AAM 进行敲降、敲除和过表达,证实其可以促进巨噬细胞活化并促进免疫应答基因(IRG)表达。在机制上,linc-AAM 通过两个 CACACA motif 与 hnRNPL 蛋白相互作用,导致后者与组蛋白 H3 解离,从而激活染色质并促进 IRG 的转录。值得注意的是,linc-AAM 敲除小鼠表现出抗原特异性细胞免疫和体液免疫反应受损。总之,本研究揭示了 lncRNA 调节 hnRNPL 功能新的分子机制,并证实linc-AAM 可以作为转录增强子激活巨噬细胞并促进适应性免疫应答。
研究结果
1. 活化巨噬细胞中 linc-AAM 的鉴定
在之前的研究中,利用欧易生物所提供的 lncRNA 芯片服务,孙红祥教授团队在 AEPS 所活化的 RAW264.7 细胞中筛选获得了 6 个上调倍数最大的 lncRNAs,后续的 RT-qPCR 实验证实其中的 linc-AAM 上调最为明显(图 A)。RT-qPCR 显示,RAW264.7 细胞经 APES 刺激后linc-AAM 表达量显著上升,同时后续伴随一系列免疫应答基因(immune response genes, IRG)表达上调(图 B)。
linc-AAM 是一个没有翻译能力、长度 1964 nt 的单外显子 lincRNA,亚细胞定位显示它主要分布于细胞核中(图 C-H)。同时 RT-qPCR 结果显示,linc-AAM 主要表达于富含免疫细胞的组织(如淋巴结、腹腔细胞、肠粘膜等,图 I)中;在 AEPS 刺激的 BMDC、BMDM 以及 PM 细胞中也显著上调(图 J);免疫刺激剂 LPS、Quil A 和 poly(I:C) 也能诱导 RAW264.7 细胞linc-AAM 显著上调(图 L)。
以上结果表明,linc-AAM 是一个免疫组织和免疫细胞特异性表达的 lncRNA,在巨噬细胞活化过程中作为早期事件被诱导表达。

活化巨噬细胞中 linc-AAM 的鉴定
2. linc-AAM 敲降或敲除可以抑制巨噬细胞活化和体内外IRG表达
利用表达谱芯片,分析 linc-AAM 敲降对 AEPS 诱导的 RAW264.7 细胞转录组表达的影响。结果显示 AEPS 刺激显著上调包括细胞因子(如 IL-1β、TNF-α、CCL22)和表面分子(如 CD40、CD80、CD86)等一系列 IRGs表达水平,而敲降 linc-AAM 可以抑制 AEPS 诱导的活性,并通过 RT-qPCR、ELISA、WB 和 FCAS 等方法得以证实(图A-D)。因为 linc-AAM 定位于细胞核,接下来利用 LongTarget 预测 linc-AAM 与上述 AEPS 诱导上调 IRGs 启动子区域的结合潜能,结果显示其中大多数 IRGs 启动子序列具有和 linc-AAM 结合的潜力。
为了排除 RNAi 敲降所导致的脱靶效应,进一步利用 CRISPR-cas9 技术构建 linc-AAM 敲除小鼠进行体内功能研究院。同样 linc-AAM 敲除也可以逆转 AEPS 诱导的 IRGs表达上调(图 F-H)。
已有的研究表明 miR155hg 和 miR-155 也可以促进巨噬细胞活化,RT-qPCR 显示 linc-AAM 敲降/敲除并不影响 miR155hg 和 miR155 的表达量,表明对于巨噬细胞的活化调控,miR-155 和 linc-AAM 是两个独立的机制(图 I-J)。

linc-AAM 敲降或敲除可以抑制巨噬细胞活化和免疫应答基因表达
3. linc-AAM 过表达促进巨噬细胞活化和 IRGs 表达
在 RAW264.7 细胞中过表达 linc-AAM,结果显示可以导致 IRGs表达上调(图 A-C),细胞吞噬活性和 NO 分泌能力显著增强(图 D-E)。同时 linc-AAM 过表达可以导致 AEPS诱导的 IRGs 表达进一步上调(图 F-G)。
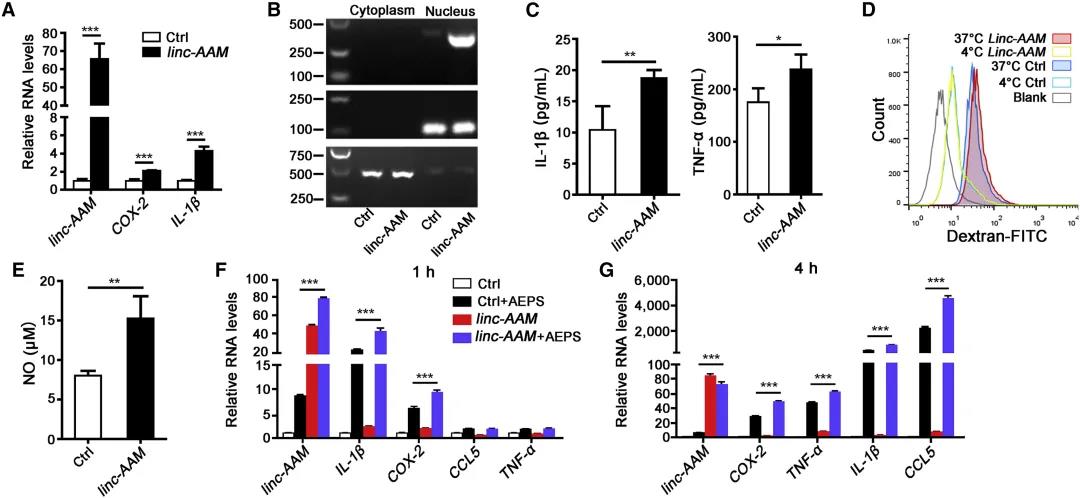
linc-AAM 过表达促进巨噬细胞活化和 IRGs 表达
4. NF-κB p65 调控巨噬细胞 linc-AAM 的表达
linc-AAM 的启动子序列预测分析表明,其转录可能受到转录因子 NF-κB 和 STATx 的调控。利用抑制剂阻断或敲降 NF-κB p65,可以显著抑制 AEPS 诱导 RAW264.7 细胞 linc-AAM 表达(图 A-D);过表达 NF-κB p65 可以上调 linc-AAM 的表达(图 E)。荧光素酶报告实验和 ChIP-qPCR 的结果表明,NF-κB p65 可以与 linc-AAM 启动子中两个位置结合以调控其转录(图 F-H)。

NF-κB p65 介导了巨噬细胞中 linc-AAM 的表达
5. linc-AAM 与 hnRNPL 互作调控 IRGs 表达
利用 RNA pull-down 富集与 linc-AAM 结合的蛋白质,通过质谱鉴定到 3 个蛋白质,并通过 WB 和 RIP-PCR 证实仅 hnRNPL 可以与 linc-AAM 特异性结合(图 A-F)。linc-AAM 序列中含有 3 个 hnRNPL 可以识别的 CACACA motif,分别突变后检验与 hnRNPL 的结合能力,结果显示其中的 CA1 和 CA3 motif 对于 hnRNPL 结合至关重要(图 G-H)。
在 RAW264.7 细胞中敲降 hnRNPL,RT-qPCR 显示 linc-AAM 表达水平没有显著变化,但 IL-6 表达水平显著上升(图 I-L);同时在 linc-AAM 敲降 RAW264.7 细胞中回补 linc-AAM表达,受损的 IL-6 和 COX-2 表达水平可以得以挽救(图 M-N),进一步证实了 linc-AAM与 hnRNPL 的互作在调控 IRGs 表达中的重要作用 。

linc-AAM 与 hnRNPL 互作以调控 IRGs 的表达
6. linc-AAM 激活染色质促进 IRGs 转录
利用组蛋白 H3 和 H3K4me3 特异性抗体进行 RIP-PCR,结果显示可以显著富集linc-AAM,表明其结合在染色质上(图 A)。RNA pull down 结果表明组蛋白 H3 与 linc-AAM 的互作依赖于 linc-AAM 上的 CACACA motif(图 B)。Co-IP 实验表明,AEPS 处理可以导致组蛋白 H3 与 hnRNPL 的结合减弱(图 C-D);linc-AAM 敲除小鼠 BMDMs 组蛋白 H3 与 hnRNPL 的结合显著增强(图 E)。
荧光素酶报告实验和 ChIRP-qPCR 结果显示,linc-AAM 可以直接与 IL-1β 等 IRGs 启动子序列结合(图 F-H)。这些结果表明,linc-AAM 可以选择性地识别靶 IRGs 的启动子序列并与 hnRNPL 结合,导致 hnRNPL 从 hnRNPL-H3 复合体中解离,进而促进 IRGs 的转录(图 I)。
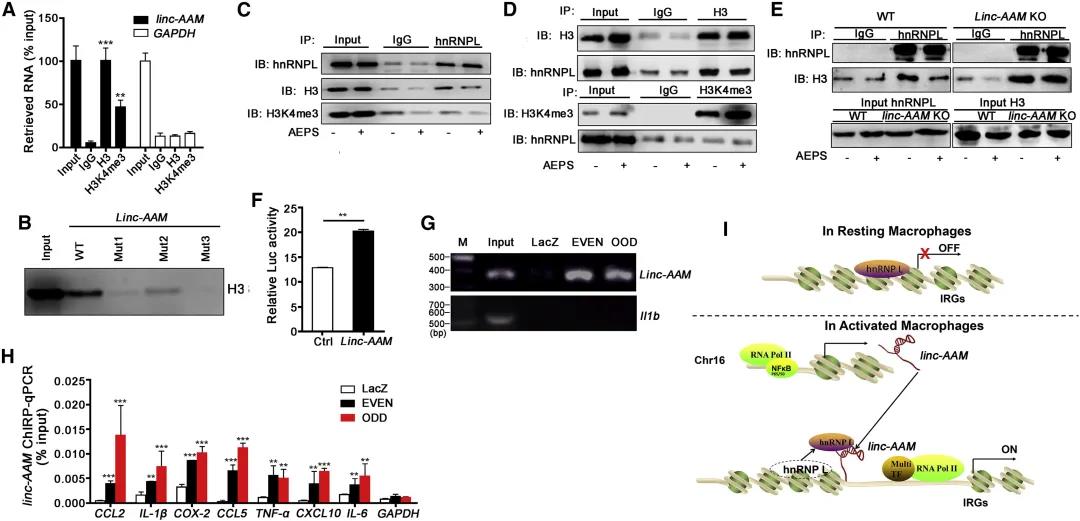
linc-AAM 激活染色质以促进 IRGs 的转录
7. linc-AAM 敲除抑制体内适应性免疫应答
最后,linc-AAM 敲除小鼠,呈现脾小体减少、变小,脾脏和胸腺指数降低,OVA 免疫小鼠血清中抗原特异性 IgG 及其亚类抗体效价降低,Con A、LPS 和抗原特异性刺激脾细胞增殖反应降低,抗原特异性刺激脾细胞细胞因子和转录因子 mRNA 表达水平下调等适应性免疫应答反应下降的表型。

linc-AAM 敲除抑制小鼠适应性免疫应答
研究结论
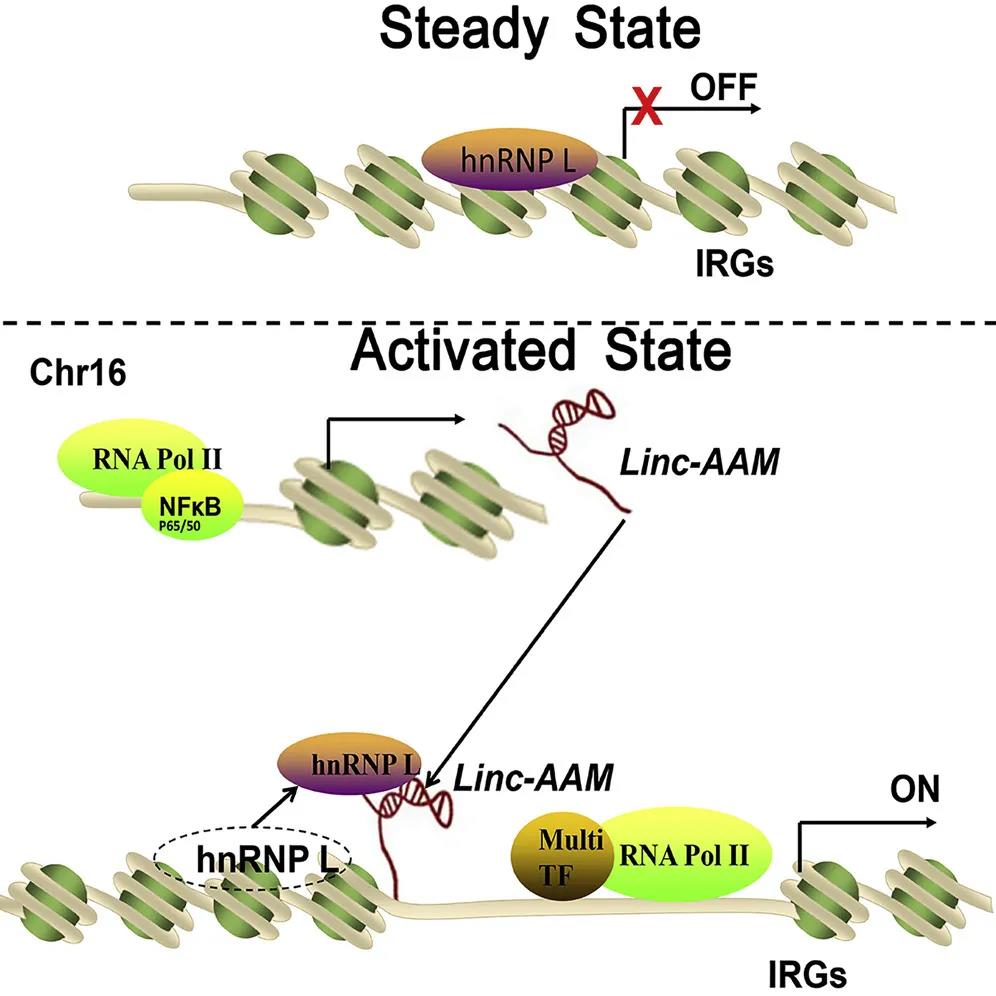
本研究报道了一个调控巨噬细胞活化和适应性免疫应答的lncRNA – linc-AAM。linc-AAM 转录受 NF-κB p65 调控。linc-AAM 在细胞核中与 hnRNPL 相互作用,使 hnRNPL 从与组蛋白 H3 结合的复合物中解离出来,进而促进 IRGs 的转录。本研究表明:lncRNA 通过影响 hnRNPL 与组蛋白 H3 的结合调控其功能。linc-AAM 有望作为自身免疫性疾病治疗和疫苗佐剂设计的新靶标。
参考文献

评论