产品详情
文献和实验
相关推荐
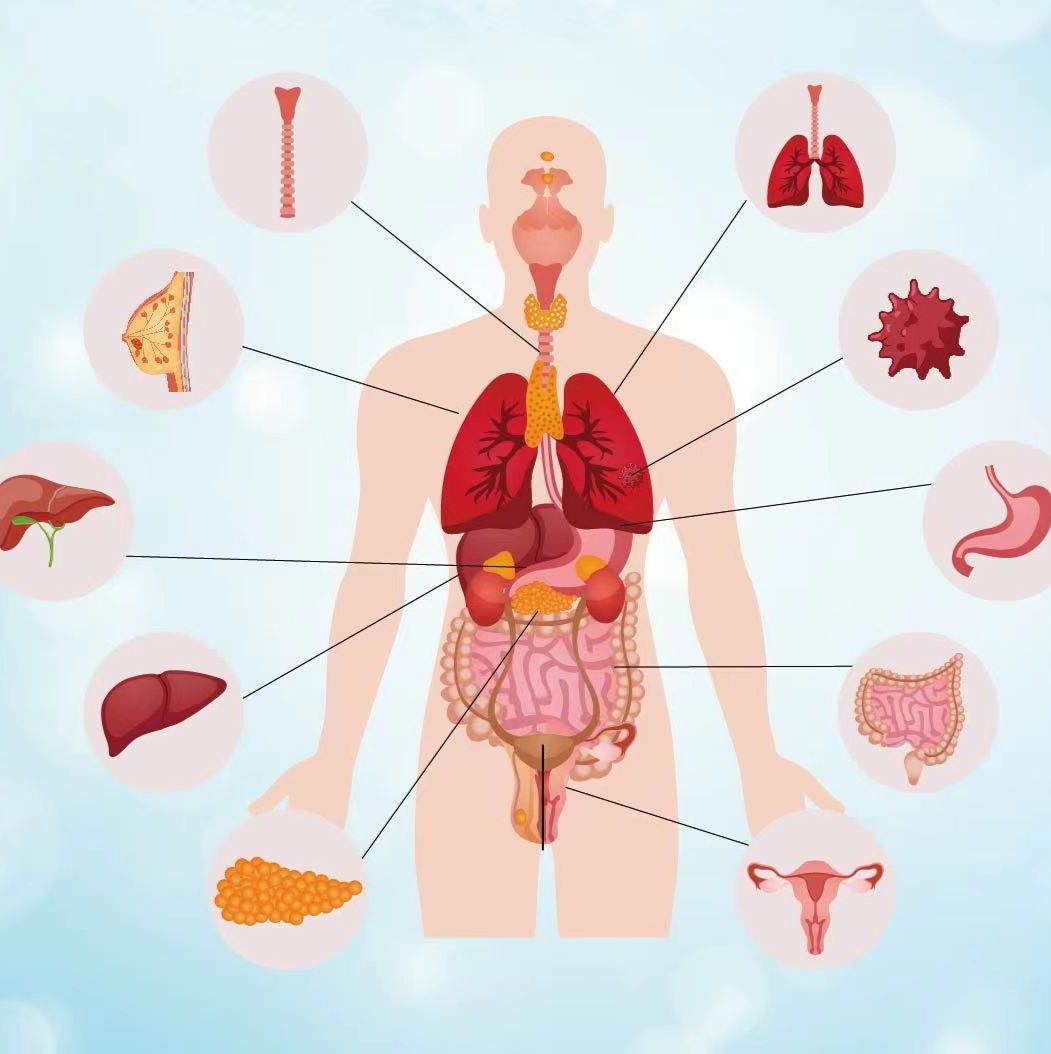
类器官(Tumor organoids)是一种体外培养的三维细胞聚集体,能够模拟实际肿瘤的微环境、结构和功能。它被Science评为2013年度十大技术;被Nature Method评为2017年度方法,喻为肿瘤患者的“试药替身”;2021年,科技部把类器官列为 “十四五“国家重点研发计划的6个重点专项之一。如果说基因检测是肿瘤精准治疗1.0时代,那类器官体外药敏分析可以称之为肿瘤精准治疗2.0时代。 表观生物联合多家领先的类器官技术公司,合力打造肿瘤类器官技术服务平台,通过引进成熟的培养技术,为医学研究领域提供类器官构建及多组学测序整体服务。目前可对外承接以下10种高发恶性肿瘤类型的类器官技术服务:
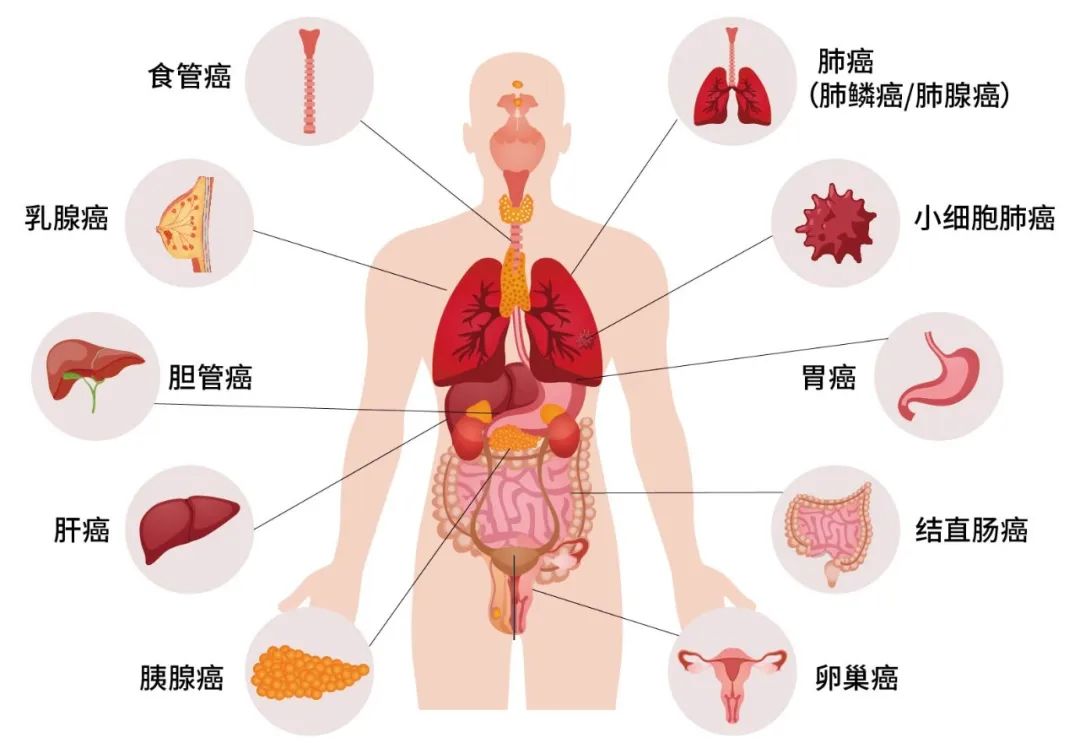
图1. 表观生物提供10种高发恶性肿瘤的类器官技术服务
技术应用
1、指导个性化精准治疗:通过构建患者特定的肿瘤类器官模型,并结合单细胞测序技术,可以对肿瘤的异质性进行深入分析,辅助医生为患者设计更加个性化的治疗方案,提高治疗的成功率和效率。
2、研究肿瘤异质性:利用类器官模型结合单细胞转录组学等多组学测序技术,可以在单细胞水平上分析肿瘤内不同细胞类型的基因表达模式,为研究肿瘤的发生、发展机制提供重要信息。
3、药物筛选和评估:类器官技术可以用于模拟人体内的肿瘤微环境,结合多组学测序技术分析药物作用机制和效果,为药物筛选和评估提供了一个高效的平台。
4、研究肿瘤进展和转移:通过从患者标本中直接提取肿瘤细胞建立肿瘤类器官生物库,并结合多组学测序技术,可以用于研究肿瘤的进展、转移以及对药物的响应。
5、探索肿瘤治疗新靶点:类器官和多组学测序技术的结合,可以在细胞和分子水平上揭示肿瘤的关键生物学过程和关键调控元件,为发现新的治疗靶点提供可能,推动新一代抗肿瘤药物的研发。
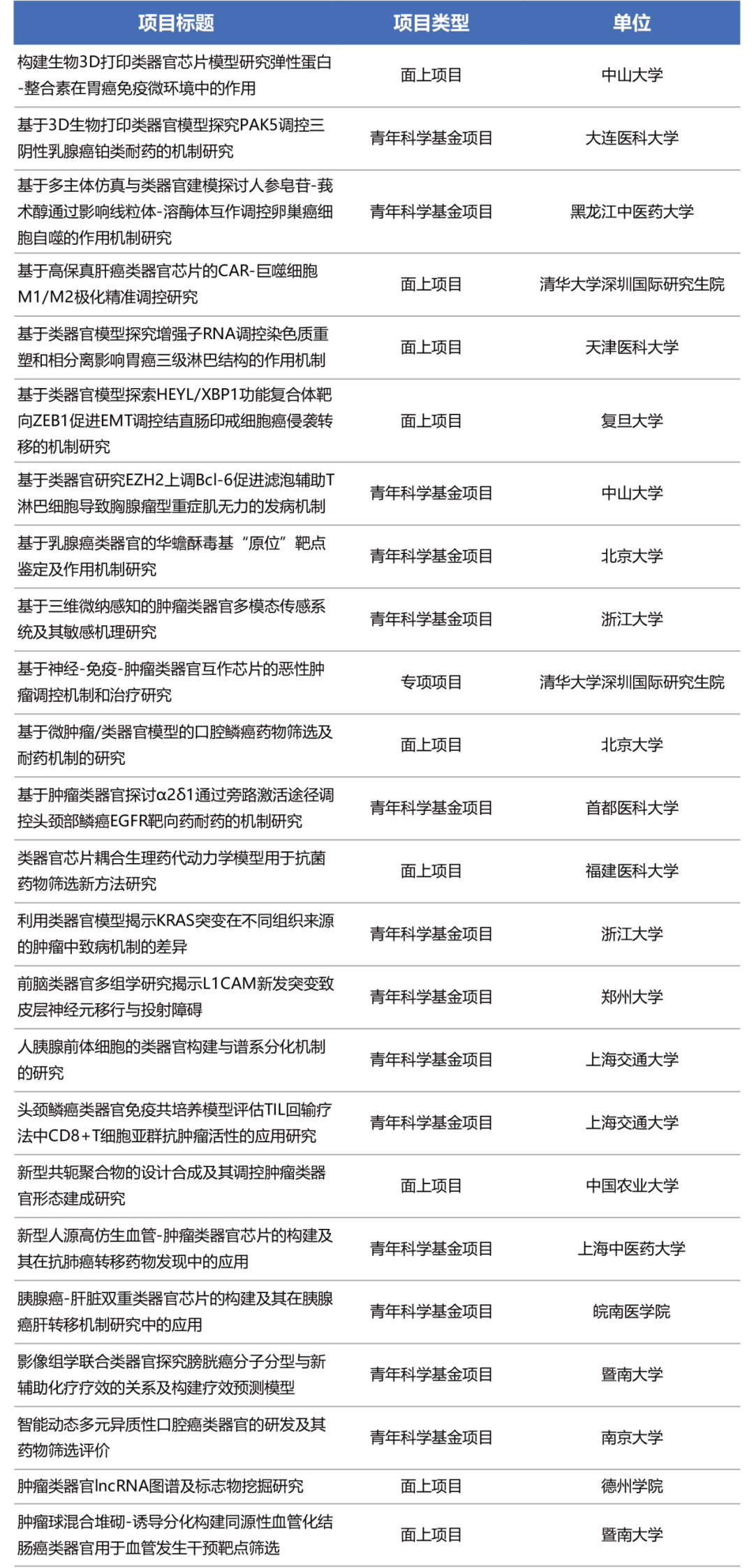
表1. 2023年NSFC肿瘤类器官相关中标课题
技术优势
1、 从类器官项目分离培养,到药物筛选和多组学测序,一站式服务 2、 结合表观遗传组学、单细胞组学等高通量测序技术,多个研究热点强强联手 3.、广泛的肿瘤类型覆盖,满足深入研究需求 4.、高成功率的技术保证,助力研究突破
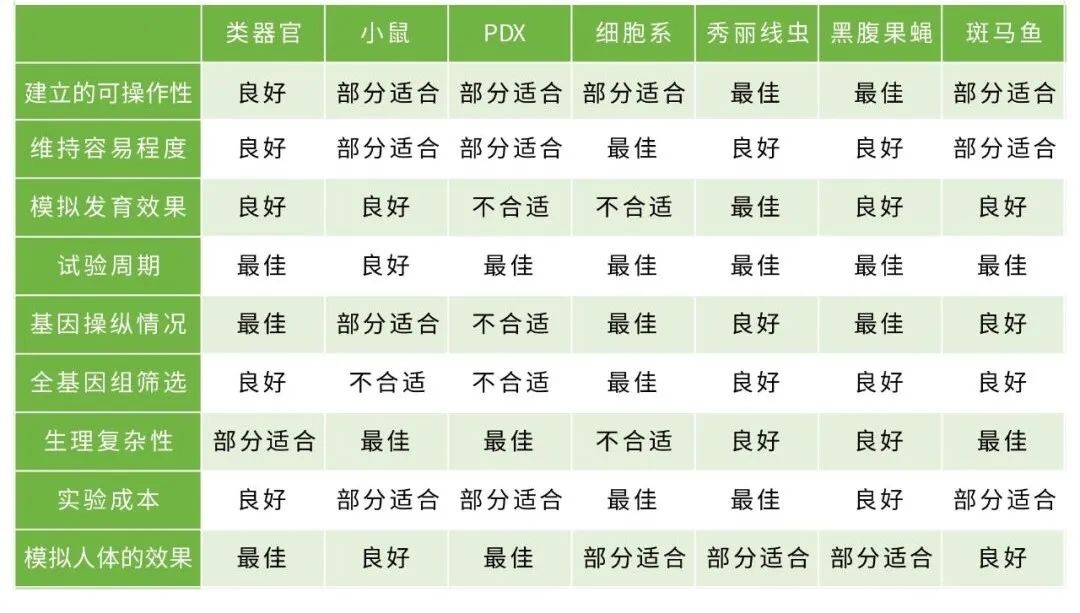
表2. 多种科研模型技术对比
肿瘤类器官精准医疗核心调控元件研究方案
类器官OrganoCT技术服务、LNA Gapmer
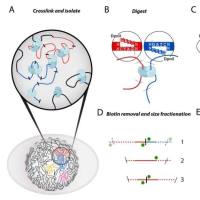
表观生物结合自身表观遗传学研究领域优势项目,推出针对类器官样本的CUT&Tag测序技术服务OrganoCT。通过OrganoCT可以描绘类器官样本全基因组的组蛋白修饰图谱,或其他转录因子结合图谱。结合超级增强子鉴定以及核心调控回路分析,筛选出核心转录因子,揭示疾病核心调控元件,有望开发特异性治疗靶点以及潜在核酸药物。

图2. 肿瘤类器官精准医疗核心调控元件研究思路
肿瘤类器官多组学联合方案
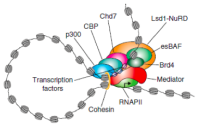
类器官DRUG-seq、SLAM-seq、EM-seq 除了OrganoCT,表观生物还提供更多肿瘤类器官多组学联合研究方案,包含多个研究热点:类器官、增强子RNA、染色质重塑、相分离,更前沿的研究方向,更尖端的解决方案! 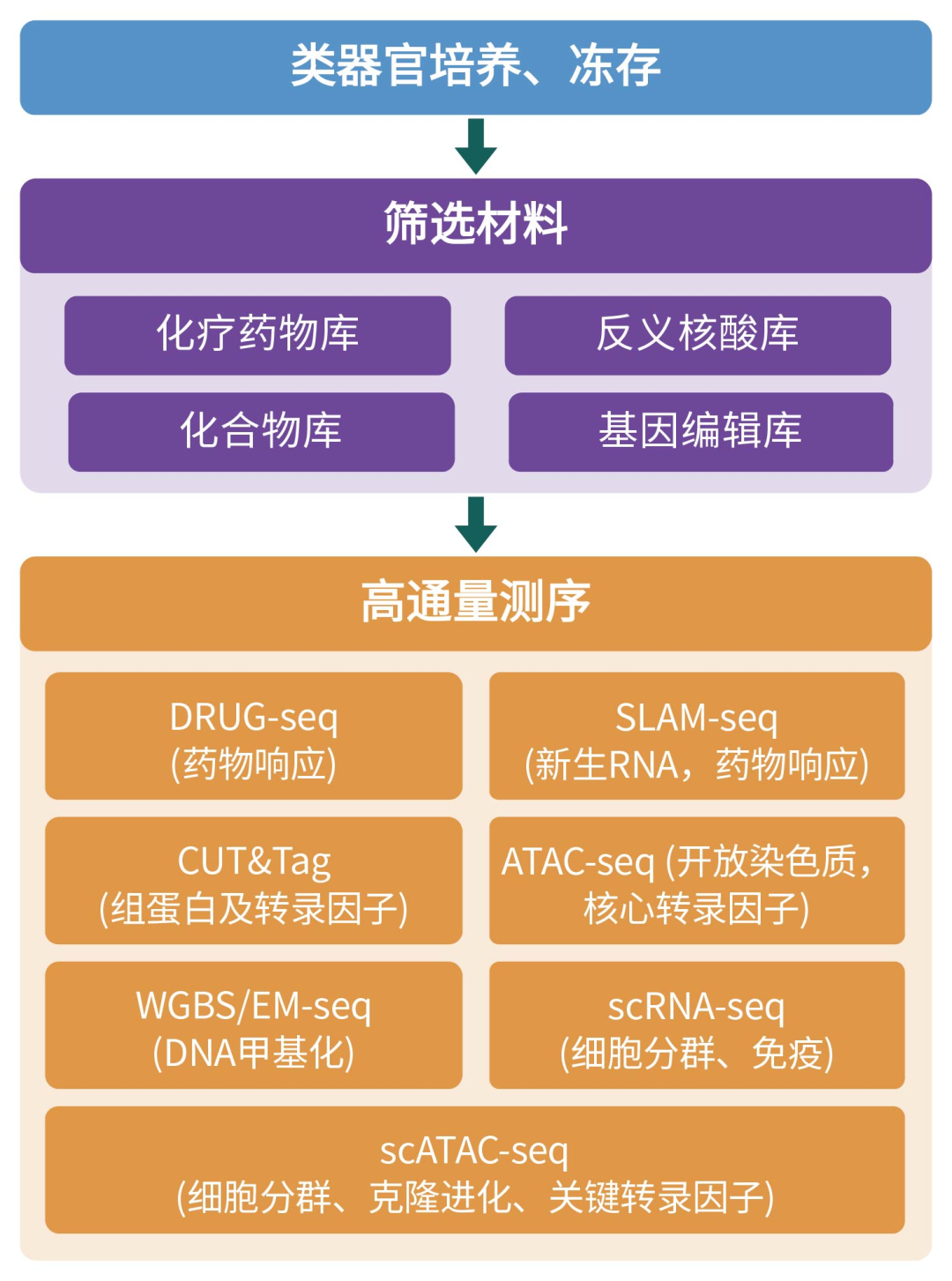
图3. 肿瘤类器官多组学联合研究思路
肿瘤类器官单细胞组学
类器官scRNA-Seq、scATAC-seq
将肿瘤组织制备成类器官后再进行单细胞测序,能够更好地保留肿瘤的异质性,模拟肿瘤的自然状态,分析细胞类型和基因表达模式,从而探究器官的异质性和疾病的分子机制,更高地指导个性化精准治疗,提升研究的精确度,深入挖掘肿瘤的遗传和表观遗传信息,为发现新的治疗靶点和药物开发提供重要线索。
案例解读
案例1 | Nat Chem Biol:类器官筛查揭示人类结直肠癌的表观遗传缺陷[1]
由于癌症患者存在基因多样性,传统的标准化治疗方案可能并不适用于每个患者。此研究建立了稳定的结肠癌类器官高通量筛选平台用于观察分子靶向药物同肿瘤的作用效果及通过检测组蛋白甲基化修饰H3K27ac、DNA甲基化分析揭露了结肠癌中的表观遗传缺陷。
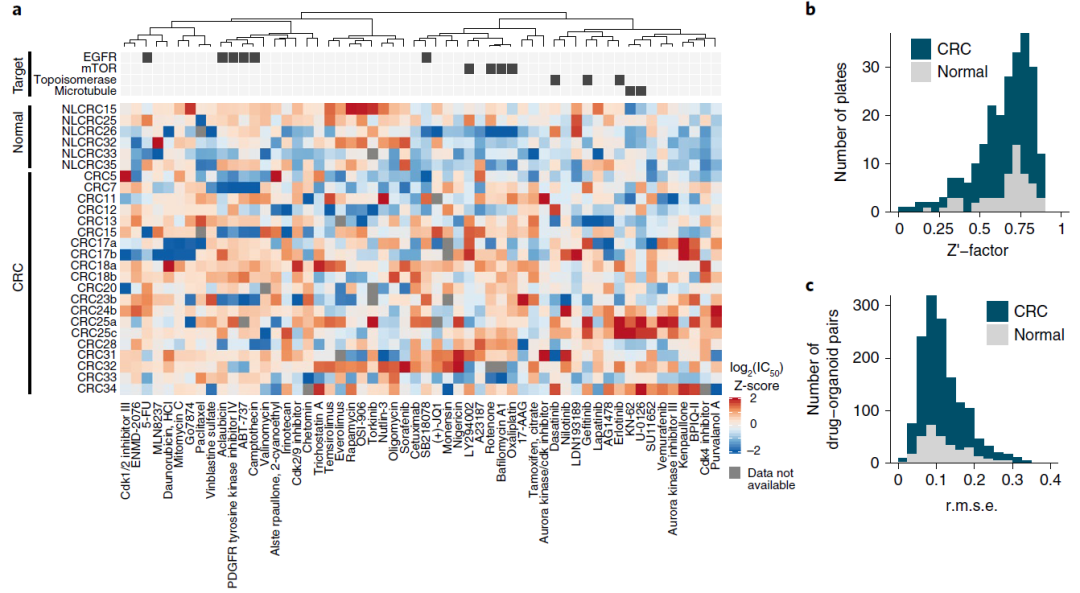
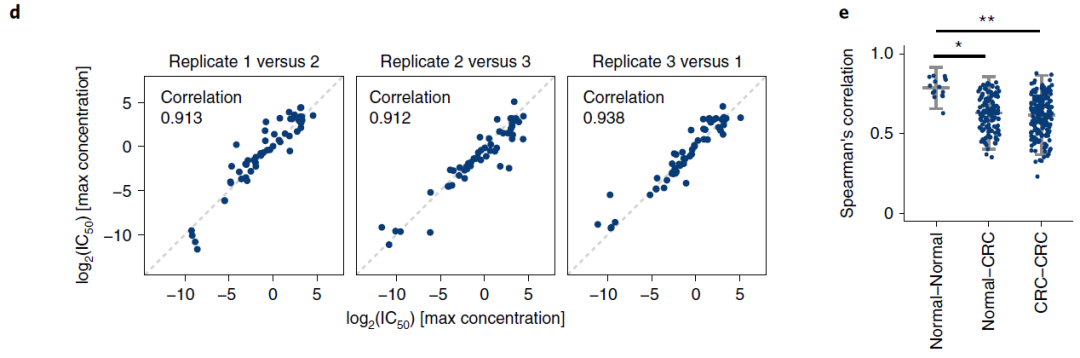
图4. 分别对结直肠癌和正常结肠类器官进行了56种药物的高通量筛选,观察对药物的敏感性
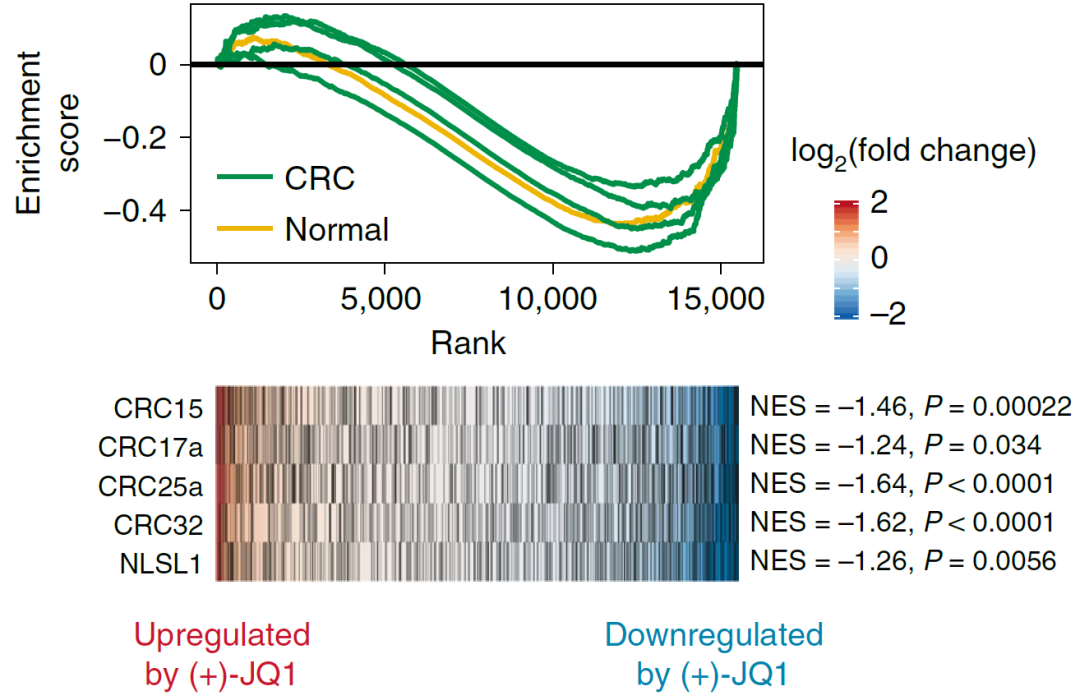
图5. 药筛实验发现JQ1能抑制类器官生长,鉴于JQ1针对的是指定组织谱系的超级增强子以癌症特异性的方式抑制类器官生JQ1为了探索具有癌症特异性的药物,研究者对结直肠癌和正常类器官进行了H3K27ac ChIP-seq检测,发现JQ1显著抑制了超增强子邻近基因的表达
案例2 | Cancer Cell:利用癌症大型类器官生物库对肿瘤内异质性进行药物基因组分析[2]
该研究建立了一个来自144例原发性肝癌患者的399个肿瘤类器官生物样本库。它概括了亲代肿瘤的组织病理学和基因组图谱,并且可以可靠地用于药物敏感性筛选。揭示了肝癌器官生物样本的肿瘤内和肿瘤间的异质性,并发现预测药物反应的生物标志物。此外,研究还强调了肝癌的广泛基因组异质性可能影响患者预后和药物反应。发现器官生物样本药物筛选能够准确预测患者对各种靶向治疗的反应,为器官生物样本在肝癌患者个体化医学中的潜在临床应用提供重要的思路与方法! 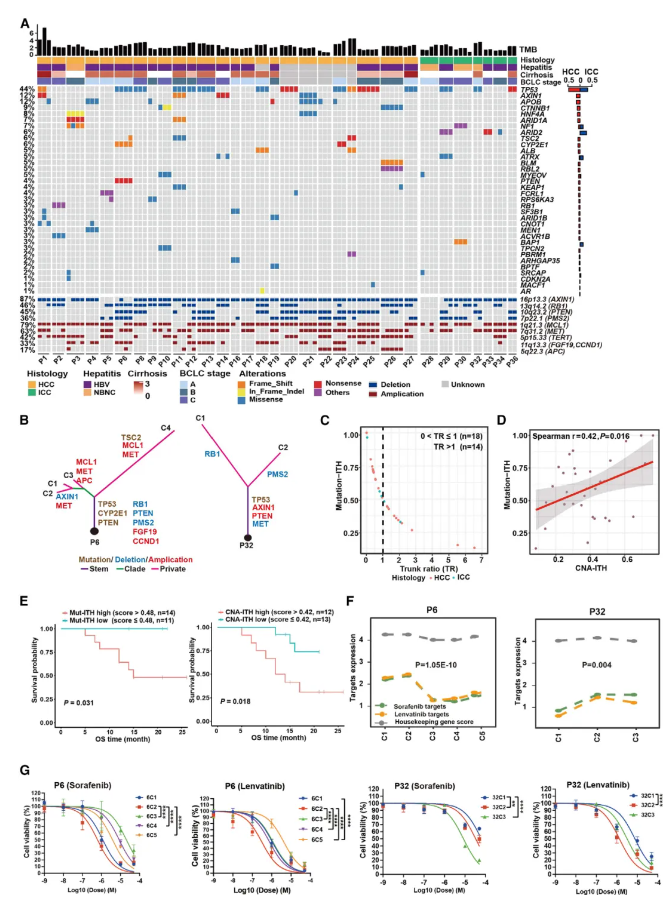 图4. 具有基因组肿瘤内异质性特征的多区域类器官分析及其相关功能意义
图4. 具有基因组肿瘤内异质性特征的多区域类器官分析及其相关功能意义
参考文献
[1] oshimitsu, K., Takano, A., Fujii, M. et al. Organoid screening reveals epigenetic vulnerabilities in human colorectal cancer. Nat Chem Biol 18, 605–614 (2022).
[2] Yang H etal. Pharmacogenomic profiling of intra-tumor heterogeneity using a large organoid biobank of liver cancer. Cancer Cell. 2024 April 8.

广州表观生物科技有限公司
实名认证
钻石会员
入驻年限:9年