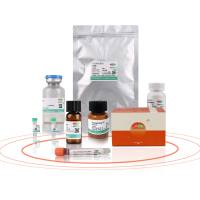
产品详情
文献和实验
相关推荐
库存 :现货
英文名 :Cell Total RNA Isolation Kit
CAS号 :-
保质期 :常温保存,有效期12个月
供应商 :爱必信(上海)生物科技有限公司
保存条件 :常温保存,有效期12个月
规格 :50T/200T
| 产品描述 | ||||||||||||||||||||||||||||
| 描述 | 11分钟即可从各种培养细胞中高效率的提取得到高纯度高质量的总 RNA。 产品特点: 1. 全程常温操作,无需冰浴和低温离心。 2. 整套试剂盒全RNase-Free,无需担心RNA降解。 3. DNA-Cleaning Column特异结合DNA,使得试剂盒无需额外添加DNase即可去除基因组DNA污染。 4. RNA得率高:RNA-only Column和独特配方搭配能高效的纯化RNA。 5. 速度快:操作简便,可在11分钟内完成。 6. 安全:无需有机试剂抽提。 7. 质量高:提取得到的RNA纯度高,没有蛋白和其他杂质污染,能够满足后续各种实验。 试剂盒组成:
|
|||||||||||||||||||||||||||
| 应用 | 适用于 从 96 、 24 、 12 、 6 孔板培养细胞总RNA提取纯化 。 | |||||||||||||||||||||||||||
| 使用方法 | 自备试剂:无水乙醇、β-巯基乙醇(选用) 使用前请先在Buffer cRL2 和Buffer RW2 中加入无水乙醇,加入体积请参照瓶上的标签 。 如提取的RNA不用于克隆全长cDNA,仅用于qPCR或测序分析等其他下游操作Buffer c RL1 可以选择不加 β 巯基乙醇,不会影响提取效果。为了避免样本间交叉污染,每次取样后都需要将取样器材的刃口或与样本直接接触的部位浸入2%sodium hypochlorite溶液中,反复洗刷数次进行清洗,然后用干净的纸巾擦干残余液体后再进行使用。为了试验方便,也可准备多个取样器材,在使用完后进行统一清洗,确保每一单独样本均使用的是无污染的取样器材。 1. 根据不同来源按以下说明进行细胞裂解。 a 贴壁细胞: 将培养皿倾斜约30°,使用移液器或移液管缓慢吸去培养基,务必彻底吸除干净,然后加入Buffer cRL1 加入量见下表进行消化、裂解 (将Buffer cRL1 完全覆盖培养皿,倾斜培养皿,使用移液器将细胞全部吹打下来);或者使用胰酶消化细胞, 离心收集细胞后参照下表加入 Buffer cRL1 (加入量见下表) 用移液器反复吹打混匀(直到看不到细胞团为止)。注意:务必将细胞培养皿中的液体彻底吸干净,否则会很大程度上影响RNA的得率和纯度。 b 悬浮细胞 直接离心收集细胞 参照下表 加入Buffer cRL1 (加入量见下表),用移液器反复吹打混匀 (直到看不到细胞团为止)。注意:RNA在Buffer cRL1 不会受到 RNase 的污染,如果细胞在加入Buffer cRL1 裂解后不即时使用,在室温条件下可保存约24 h,在 4°C 中保存约1周,更长时间保存请存放于 -80℃,使用时将溶液在室温或37℃ 溶解即可。 表:细胞数量与试剂使用量关系列表。
2. 将裂解好的细胞混合液转移至DNA-Cleaning Column 中 (DNA-Cleaning Column放入收集管中),12,000 rpm (~13,400 ×g ) 离心2 min。 移除DNA-Cleaning Column,保留收集管内上清液。注意:如果DNA-Cleaning Column 收集管底部有沉淀产生,请将上清液转移至干净离心管中再进行步骤3,切勿将其吸入上清液中。 3. 向 上述 上清液中加入 1. 6 倍体积 Buffer c RL2 (加入量见上表) (使用前请确认已按照说明加入无水乙醇),轻柔混匀。注意:Buffer cRL2 加入量请按照实际操作过程中上清液的体积进行比例换算加入。例如:250 ul上清液中加入400 ul Buffer cRL2 (已加入无水乙醇)。如果混合液出现浑浊或絮状沉淀,请直接进行步骤4即可。 4. 将混合液全部转移至RNA-only Column 中 (纯化柱放入收集管中),12,000 rpm (~13,400 ×g ) 离心1 min弃掉收集管中的废液。注意: 如果混合液中出现 絮状 沉淀,请将沉淀一并转移至纯化柱中。若细胞数量为6 孔板或3.5 cm板,请分两次将混合液全部过柱。 5. 向纯化柱中加入500 ul Buffer RW1,12,000 rpm (~13,400 ×g ) 离心1 min弃掉收集管中的废液。 6. 向纯化柱中加入700 ul Buffer RW2 (使用前请确认已按照说明加入无水乙醇),12,000 rpm (~13,400 ×g ) 离心1 min弃掉收集管中的废液。 7. 重复步骤 6 。 8. 将纯化柱放回收集管中,12,000 rpm (~13,400 ×g ) 空管离心2 min ,去掉离心柱中残余的Buffer RW2 。 9. 将纯化柱转移至新的RNA收集管中, 向纯化柱 的 膜 中 央 滴加20-50 ul 已于65°C 预热的RNase-Free ddH2O (切勿将洗脱液添加到压圈上,否则会损失较大体积的洗脱液),室温放置2 min。12,000 rpm (~13,400 ×g ) 离心1 min 收集RNA溶液。注意:硅胶膜会吸附少量的液体,洗脱后所得的RNA产物体积会有所偏差。增加洗脱体积可提高RNA产量,RNase-Free ddH2O 加入体积不应低于20 ul,体积过小会影响洗脱效率。得到的RNA溶液可直接用于下游实验或置于80°C保存。 由于本试剂盒对RNA二级结构保护较好,建议凝胶电泳之前,先将得到的RNA溶液置于72°C 变性处理5-10min。 10. 将离心得到的RNA溶液重新加至纯化柱中,重复步骤9 (如对 RNA 得率要求不高,可忽略此步骤)。 操作示意图: 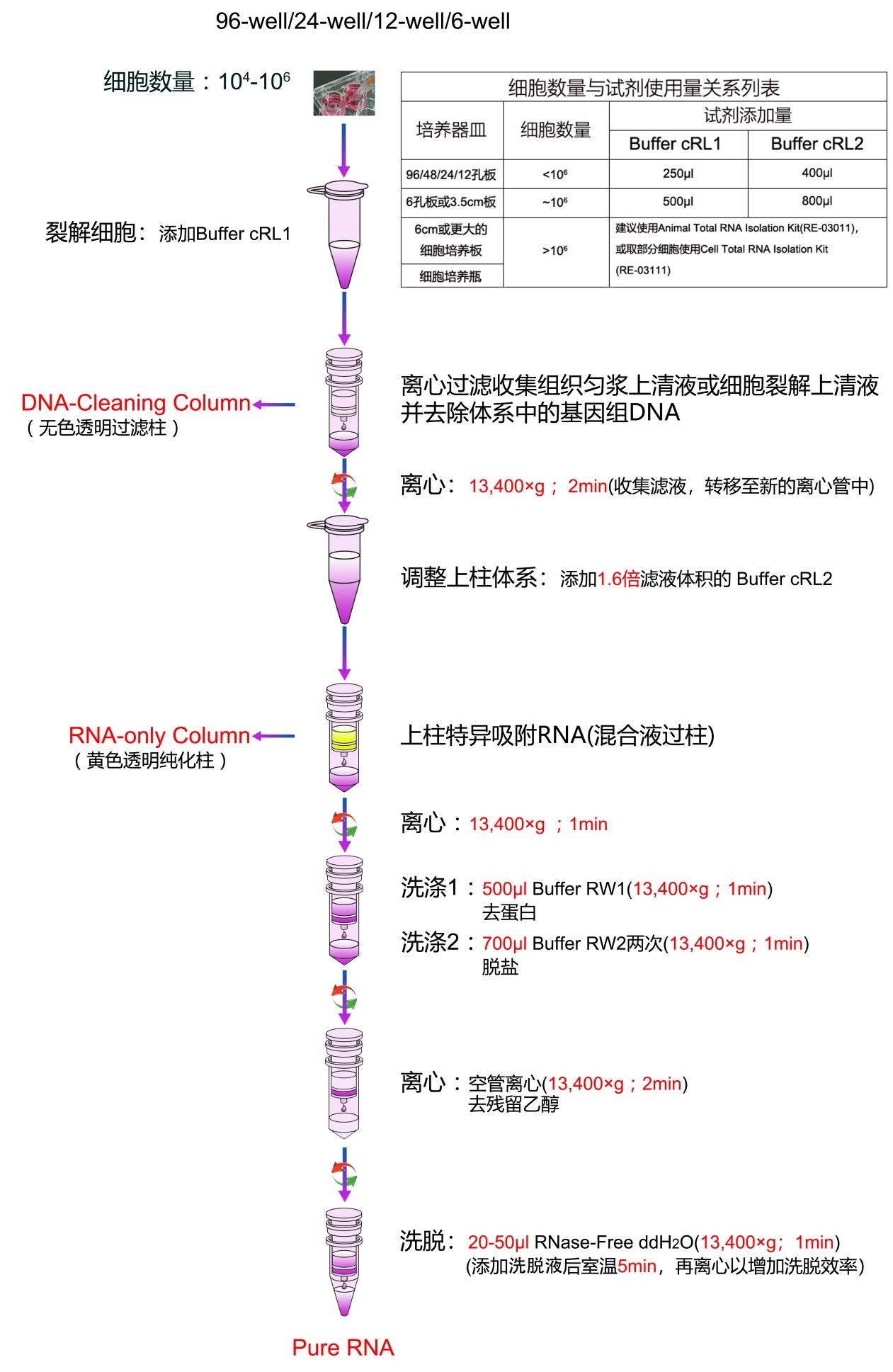 |
|||||||||||||||||||||||||||
| 储存/保存方法 | 常温保存,有效期12个月 | |||||||||||||||||||||||||||
| 技术指标 | RNA提取得率与纯度: 使用Cell Total RNA Isolation Kit 纯化得到的 RNA ,其产量与 细胞 初始量、新鲜程度、细胞 保存时间以及操作相关。以下是使用该试剂盒提取 RNA ,几种培养细胞 RNA 得率与纯度,实际操作中,可能与该数据有些许出入。
注:硅胶膜会吸附少量的液体,洗脱后所得的RNA产物体积会有所偏差。 |
|||||||||||||||||||||||||||
| 注意事项 | 1. 所有实验步骤均在常温(15-25°C) 进行 包括离心切勿使用冰浴和低温 (4°C ) 离心 。 2. 样品应避免反复冻融,否则会导致提取的RNA降解 且提取量也会下降。 3. 试剂盒使用前,请在Buffer c RL1 中加入β-巯基乙醇。每 1ml Buffer cRL1 加入10 ul β-巯基乙醇, 建议现配现用,Buffer cRL1 在加入β-巯基乙醇后可在4°C放置1个月。如提取的RNA不用于克隆全长 cDNA,仅用于qPCR或测序分析等其他下游操作,可以选择不加β-巯基乙醇,不会影响提取效果。 4. 试剂盒使用前,请在Buffer cRL2 中添加无水乙醇,加入量请参照试剂瓶上标签。不同规格的试剂盒无水乙醇的添加量见下表:
5. 试剂盒使用前,请在Buffer RW2 中添加无水乙醇,加入量请参照试剂瓶上标签。不同规格的试剂盒无水乙醇的添加量见下表:
6. RNA产率和质量与细胞样本用量和洗脱体积有关, 建议每250 ul Buffer cRL1 使用细胞的量不超过106。 7. 洗脱体积:洗脱液体积不应少于20 ul,否则会影响RNA回收效率 。 8. 请检查试剂盒中的Buffer cRL1 和Buffer RW1 是否有晶体析出现象,若低温存放后有晶体析出,可将Buffer放置于室温或37°C 一段时间,将晶体溶解后混匀再使用。 |
|||||||||||||||||||||||||||
实验结果图:

培养细胞总RNA提取试剂盒处理不同数量的细胞样本,获得的RNA电泳图。
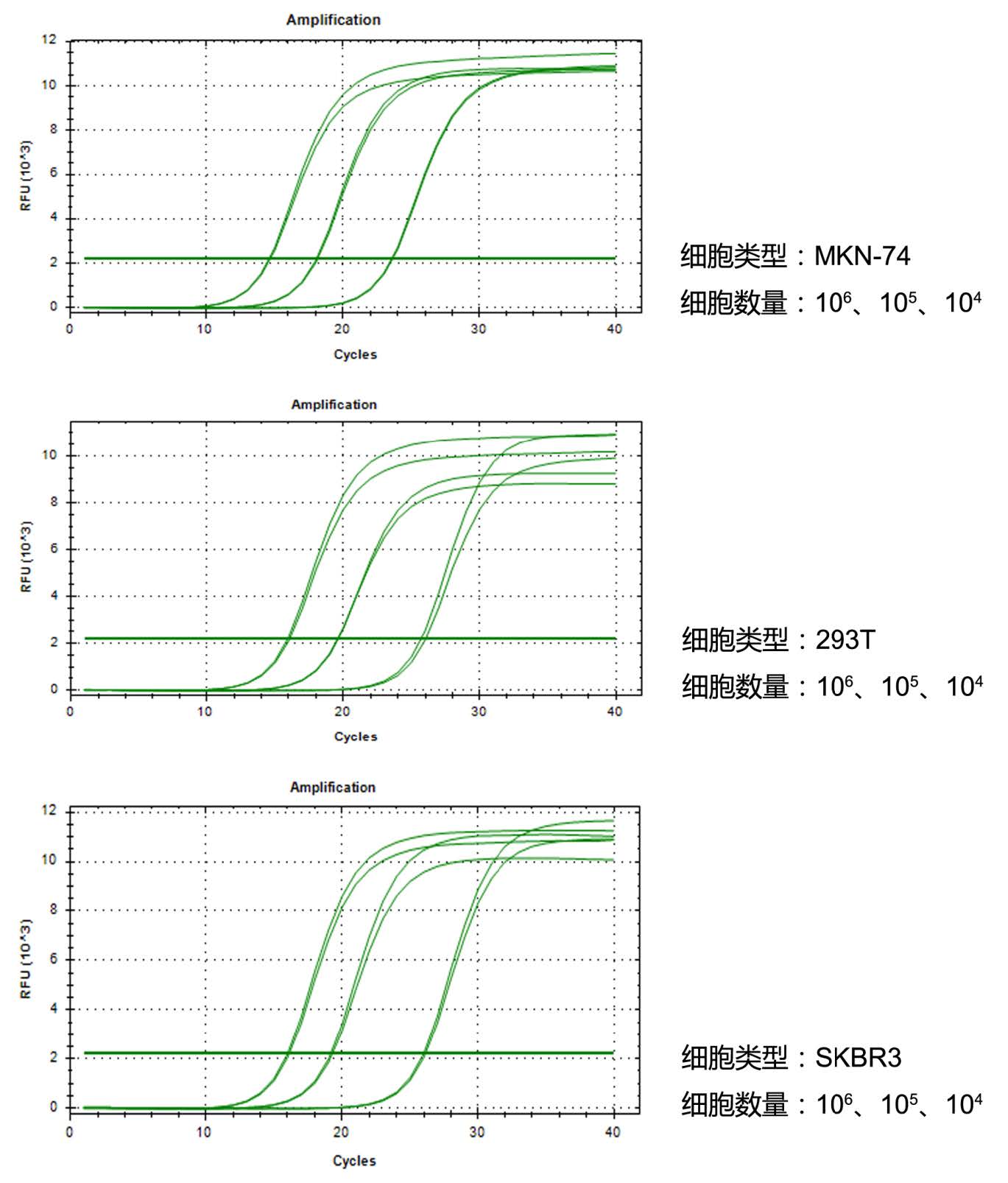
培养细胞总RNA提取试剂盒提取不同细胞的总RNA,反转录之后检测基因A的qPCR图谱 。

培养细胞总RNA提取试剂盒提取不同细胞的总RNA,反转录之后检测基因A的qPCR图谱 。

爱必信(上海)生物科技有限公司
品牌商实名认证
钻石会员
入驻年限:12年