产品详情
文献和实验
相关推荐
保存条件 :2-8°C
库存 :1000
供应商 :PROGEN Biotechnik GmbH
规格 :96 tests
AAV在基因治疗领域的应用及常用病毒滴度检测方法AAV是细小病毒科的单链DNA缺陷型病毒,有12种血清型,通常需要辅助病毒(腺病毒、疱疹病毒等)的辅助才能完成复制和装配。基因组由反向末端重复序列(ITRs)、Rep和Cap基因组成。ITRs是病毒包装复制的起点,Rep是编码病毒复制和整合蛋白的基因,Cap编码衣壳蛋白的基因。
重组AAV(rAAV)在野生AAV基础上进行改造,衣壳仍然使用野生型序列,但基因组中的Rep和Cap基因被引入的目的基所替代,仅保留ITRs和包装信号序列,因此rAAV在极大程度上降低了免疫原性、提高了安全性、是基因治疗的主要载体。
rAAV在基因治疗应用中的优点:
- 非致病性,安全性高
- 基因表达持续时间长
- 低细胞毒性,低免疫原性
- 不易整合到基因组,基因自发突变低
- 能够感染多数组织和细胞
不同血清型的组织靶向性
非致病型病毒,安全性高
基因表达持续时间较长

重组腺相关病毒(rAAV)载体是一种十分有前景的治疗方法。然而作为治疗型载体,潜在免疫毒性是研发转化为临床应用要解决的首要问题,这种免疫毒性以机体产生针对AAV衣壳抗原不良免疫反应的形式存在,而产生的原因可能是因空衣壳病毒缺少目的基因所致。因此在临床应用中,准确地定量AAV基因组滴度、感染滴度、AAV衣壳总滴度对降低免疫原性、提高安全性和有效性十分重要。
常用的AAV滴度检测方法
常用的方法包括:ELISA、qPCR、ddPCR、细胞转导、血小板测定、斑点印记、电子显微等技术。
不同检测方法检测的参数不同,例如:qPCR、ddPCR检测的是AAV基因组滴度,也称物理滴度;细胞转导法检测的是病毒感染滴度,也称功能滴度;电镜技术检测的是空衣壳与完整衣壳的比率;ELISA和斑点杂交法测定的是完整病毒颗粒(空衣壳和完整衣壳)的浓度,但斑点杂交法是半定量法,不能对衣壳滴度进行准确定量。qPCR、ddPCR操作简单快速,可实现高通量检测,但在样品处理、标准品稀释、引物设计、引物结合、PCR扩增等过程中容易产生数据差异,低温电镜检测不适用于AAV绝对定量,且设备昂贵、样品前处理复杂、检测时也容易出现伪影致使实验结果不准确。因此,比较推荐是PCR(qPCR或ddPCR)结合ELISA法,分别检测含病毒DNA的衣壳滴度和总衣壳滴度,通过计算获得空壳与全病毒的比率。
不同检测方法在检测参数、准确度和数据差异上的比较
| 检测方法 | 检测参数 | 滴度描述 | 感染滴度 | DNA滴度 | 衣壳滴度 | 准确度 | 数据差异 |
| ELISA | 总衣壳滴度(完整衣壳&空衣壳) | 完整病毒颗粒浓度(完整衣壳和空衣壳) | √ | 高 | 小 | ||
| qPCR | AAV DNA滴度 | 含病毒DNA的衣壳浓度 | √ | 中等 | 大 | ||
| ddPCR | AAV DNA滴度 | 含病毒DNA的衣壳浓度 | √ | 中等偏上 | 中等 | ||
| 细胞转导检测 | AAV感染滴度 | 转导细胞的病毒颗粒浓度 | √ | ||||
| 斑点印记 | 总衣壳滴度(完整衣壳&空衣壳) | 所有病毒颗粒浓度(完整衣壳和空衣壳) | √ | 中等 | 中等 | ||
| 电子显微技术 | 空衣壳与完整衣壳比率 | 空衣壳与完整衣壳的比率计算 | √ | 低 | / |
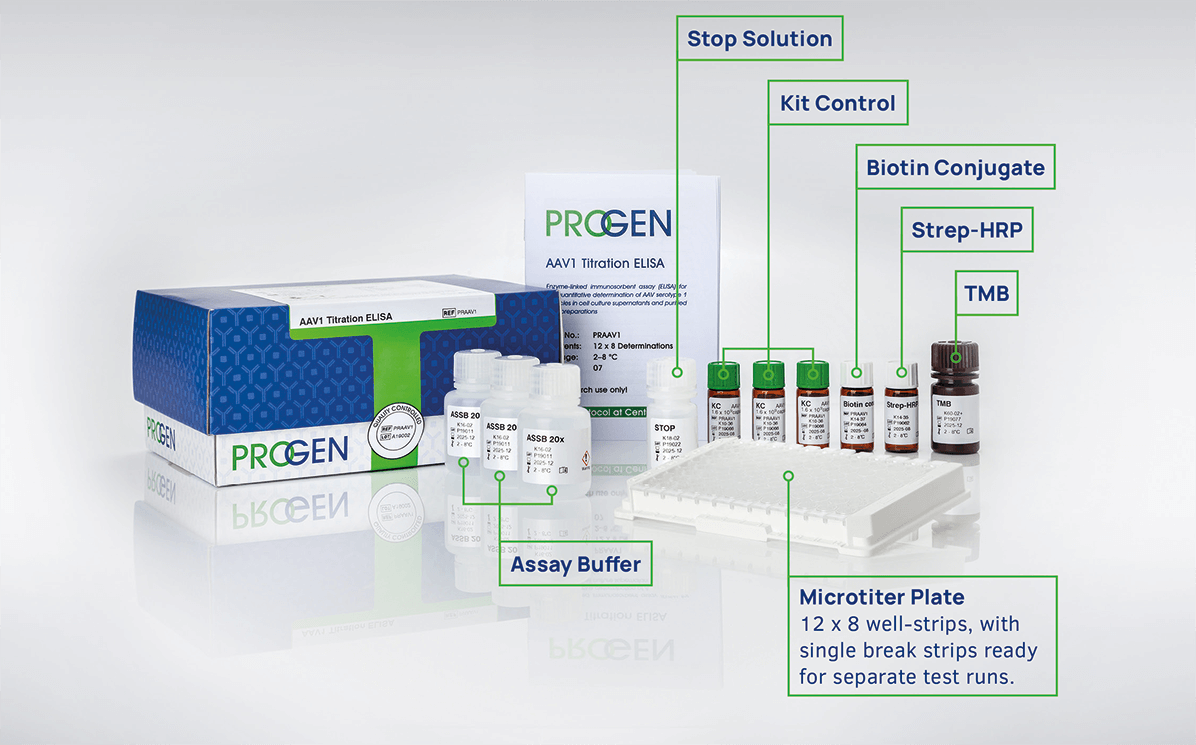
Progen AAV滴度检测试剂,基于夹心ELISA法,使用生物素标记的抗体捕获样本中的AAV病毒,通过显色法,定量检测AAV病毒滴度,产品因其操作简单、定量准确、质量稳定被基因治疗研究客户高度认可。
北京百普洛科技有限公司是PROGEN在中国的授权代理商,以提供优质的产品和完善的服务为使命,依托PROGEN在生命科学和基因治疗领域的强大专业背景,自成立以来已经为国内140多家基因治疗研发企业提供了高质量产品。

北京百普洛科技有限公司
代理商实名认证
金牌会员
入驻年限:2年