库存 :100
国食药监械注册号 :无
保修期 :12个月
现货状态 :30天
供应商 :玉研科学仪器公司
规格 :请来电咨询
据D'Amour&Smith介绍,这种新型甩尾装置用于通过对大鼠尾巴进行热刺激,能够快速精确地筛选镇痛药物而设计,见参考文献。它主要部件由一个强度可调的辐射能I.R.源,通过抛物面反射镜聚焦在鼠尾上。
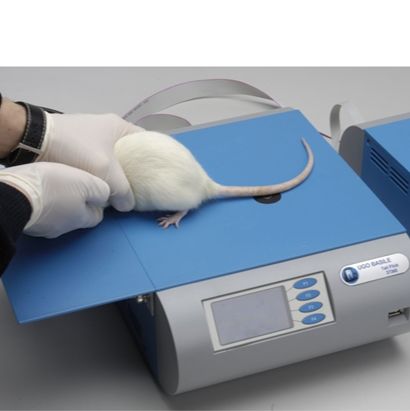
操作员将大鼠固定在无阻碍的仪表上面板(见图),使其尾部位于嵌入式窗口上,接收I.R.能量。
操作员启动刺激和相关的固态秒计数器。当老鼠感到疼痛并摆动尾巴时,传感器会检测到疼痛,停止秒计数器并关闭灯泡。因此,动物的反应时间被确定并自动记录。

主要主要特点
l 自动检测动物的反应
l 数据可传输到 U 盘或 PC (USB)
l 舒适、无阻碍的工作表面(无突出元件)
l 由于光学元件固定在刚性结构中以及由电子控制的 I.R.流量,因此具有优异的再现性。
仪器描述
仪器部件整齐地排列在一个新设计的盒子里,盒子里包括I.R.源、传感器、微控制器和电子电路。
当计数器停止时,在指示的时间保持冻结显示。延迟时间因此被自动记录。
一个倾斜的小鼠固定器作为可选件提供,配合小鼠一起使用以补偿其将尾巴保持在 45 度向上从而远离热源的趋势。
事实上,具有特定基因消除的小鼠的可用性正在推动从大鼠到小鼠作为研究动物的重大转变。

可选配的小鼠固定器

正在对大鼠进行甩尾测试

控制面板
数据采集
37360 是微处理器控制的单元。存储在其内部存储器中的实验数据可以直接导出到PC USB 或串行端口。
通信由包括在标准配置中的专用CUB数据采集软件包Cat.52050-09管理。
基于 CUB Windows® 的软件包使用户能够将实验数据传送到 PC 并将它们存储到单独的文件中,由市面上大多数统计分析软件进行管理。
37360 配备了一个存储键,用于记录一个或多个会话的所有实验数据,并从远程 PC 对实验布局进行编程。
校准辐射计
每个足底测试装置都通过校准辐射计精确校准。校准辐射计货号 37300。
终端用户应该考虑这个非常有用的可选附件,它使实验者能够:
i) 确保两个或多个装置提供完全相同强度的热伤害性刺激(以 mW/cm2 表示)。
ii) 测量 I.R. 能量(1s 持续时间内的 1mW 对应于 1mJ)的绝对值。
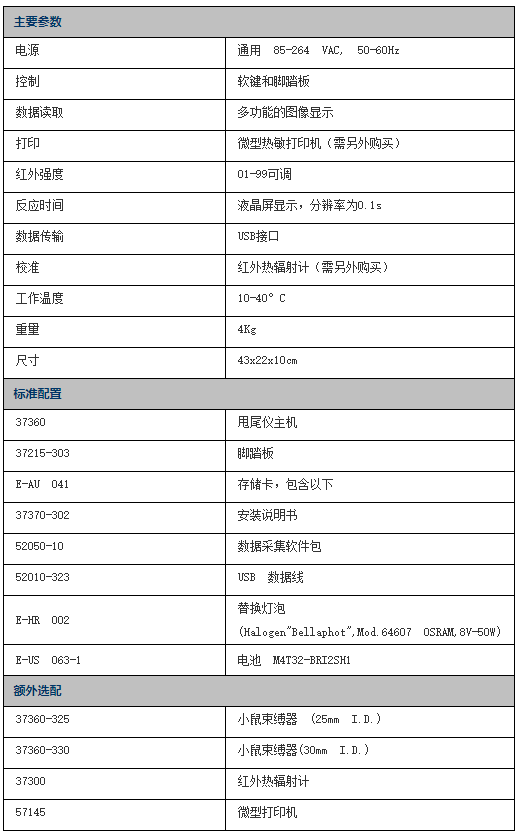
主要技术参数:
参考文献:





敬请来电咨询。
敬请关注玉研仪器微信号:yuyanbio

您想了解更多详细资料吗?
请与我们联系:
TEL : 021-35183767 , 18502129044
QQ : 3007536624
Mail: yuyan0317@126.com
敬请来电咨询!
该产品被引用文献
1.Weldon C, Ji T, Nguyen MT, et al. Nanoscale Bupivacaine Formulations To Enhance the Duration and Safety of Intravenous Regional Anesthesia. ACS Nano. 2019;13(1):18-25. doi:10.1021/acsnano.8b05408(IF=17.1)
2.Guo W, Fan S, Xiao D, et al. A Brainstem reticulotegmental neural ensemble drives acoustic startle reflexes. Nat Commun. 2021;12(1):6403. Published 2021 Nov 4. doi:10.1038/s41467-021-26723-9(IF=16.6)
3.Guida F, Boccella S, Belardo C, et al. Altered gut microbiota and endocannabinoid system tone in vitamin D deficiency-mediated chronic pain. Brain Behav Immun. 2020;85:128-141. doi:10.1016/j.bbi.2019.04.006(IF=15.1)
4.Huang F, Chen X, Jiang X, et al. Betaine ameliorates prenatal valproic-acid-induced autism-like behavioral abnormalities in mice by promoting homocysteine metabolism. Psychiatry Clin Neurosci. 2019;73(6):317-322. doi:10.1111/pcn.12833(IF=11.9)
5.Liu Q, Su LY, Sun C, et al. Melatonin alleviates morphin*e analgesic tolerance in mice by decreasing NLRP3 inflammasome activation. Redox Biol. 2020;34:101560. doi:10.1016/j.redox.2020.101560(IF=11.4)
6.Caputi FF, Rullo L, Acquas E, Ciccocioppo R, Candeletti S, Romualdi P. Evidence of a PPARγ-mediated mechanism in the ability of Withania somnifera to attenuate tolerance to the antinociceptive effects of morphin*e. Pharmacol Res. 2019;139:422-430. doi:10.1016/j.phrs.2018.11.033(IF=9.3)
7.Stone AE, Scheuermann SE, Haile CN, et al. Fentany*l conjugate vaccine by injected or mucosal delivery with dmLT or LTA1 adjuvants implicates IgA in protection from drug challenge. NPJ Vaccines. 2021;6(1):69. Published 2021 May 13. doi:10.1038/s41541-021-00329-0(IF=9.2)
8.Elhenawy AA, Al-Harbi LM, El-Gazzar MA, et al. Naproxenylamino acid derivatives: Design, synthesis, docking, QSAR and anti-inflammatory and analgesic activity. Biomed Pharmacother. 2019;116:109024. doi:10.1016/j.biopha.2019.109024IF=7.5)
9.Hu ZJ, Han W, Cao CQ, Mao-Ying QL, Mi WL, Wang YQ. Peripheral Leptin Signaling Mediates Formalin-Induced Nociception. Neurosci Bull. 2018;34(2):321-329. doi:10.1007/s12264-017-0194-2(IF=5.6)
10.Abdelkader NF, Ibrahim SM, Moustafa PE, Elbaset MA. Inosine mitigated diabetic peripheral neuropathy via modulating GLO1/AGEs/RAGE/NF-κB/Nrf2 and TGF-β/PKC/TRPV1 signaling pathways. Biomed Pharmacother. 2022;145:112395. doi:10.1016/j.biopha.2021.112395(IF=7.5)
11.Marabese I, Boccella S, Iannotta M, et al. Metabotropic glutamate receptor subtype 7 in the dorsal striatum oppositely modulates pain in sham and neuropathic rats.Neuropharmacology. 2018;135:86-99. doi:10.1016/j.neuropharm.2018.03.003(IF=4.7)
12.Suzuki T, Sawada T, Kawai K, Ishihara Y. Pharmacological profile of TAN-452, a novel peripherally acting opioid receptor antagonist for the treatment of opioid-inducedbowel syndromes. Life Sci. 2018;215:246-252. doi:10.1016/j.lfs.2018.07.028(IF=6.1)
13.De Caro C, Raucci F, Saviano A, et al. Pharmacological and molecular docking assessment of cryptotanshinone as natural-derived analgesic compound. Biomed Pharmacother. 2020;126:110042. doi:10.1016/j.biopha.2020.110042(IF=7.5)
14.Palazzo E, Boccella S, Marabese I, et al. Homo-AMPA in the periaqueductal grey modulates pain and rostral ventromedial medulla activity in diabetic neuropathic mice. Neuropharmacology. 2022;212:109047. doi:10.1016/j.neuropharm.2022.109047(IF=4.7)
15.Weber L, Wang X, Ren R, et al. The Development of a Macromolecular Analgesic for Arthritic Pain. Mol Pharm. 2019;16(3):1234-1244. doi:10.1021/acs.molpharmaceut.8b01197(IF=4.9)
16.Sasaguri T, Taguchi T, Murata Y, et al. Interleukin-27 controls basal pain threshold in physiological and pathological conditions. Sci Rep. 2018;8(1):11022. Published 2018 Jul 23. doi:10.1038/s41598-018-29398-3(IF=4.6)
17.Komatsu A, Miyano K, Nakayama D, et al. Novel Opioid Analgesics for the Development of Transdermal Opioid Patches That Possess Morphin*e-Like Pharmacological Profiles Rather Than Fentany*l: Possible Opioid Switching Alternatives Among Patch Formula. Anesth Analg. 2022;134(5):1082-1093. doi:10.1213/ANE.0000000000005954(IF=5.7)
18.Groemer TW, Triller A, Zeilhofer HU, Becker K, Eulenburg V, Becker CM. Nociception in the Glycine Receptor Deficient Mutant Mouse Spastic. Front Mol Neurosci. 2022;15:832490. Published 2022 Apr 25. doi:10.3389/fnmol.2022.832490(IF=4.8)
19.Poznański P, Lesniak A, Bujalska-Zadrozny M, Strzemecka J, Sacharczuk M. Bidirectional selection for high and low stress-induced analgesia affects G-protein activity. Neuropharmacology. 2019;144:37-42. doi:10.1016/j.neuropharm.2018.10.014(IF=4.7)
方法学文献:
F.E. D’mour & D.L. Smith: "A Method for Determining Loss of Pain Sensation." J. Pharmacol. Exp. Therap. 72: 74-79, 1941.