生活方式、肥胖和肠道微生物组是代谢异常的重要危险因素。肠道菌群与糖尿病之间也有着许许多多的关联。微生物学家赵立平教授曾经说过,我们体内的基因,一部分来自于我们的父母,还有一部分是我们身体中共生微生物从环境中带到身体中来的基因,这些基因环境互作一起在影响着我们的生老病死。人类的肠道菌群十分复杂,糖尿病与肠道菌群的关系,近些年来也一直是研究的热点。
2020 年 7 月 2 日,慕尼黑工业大学 Sandra Reitmeier 等科研人员在 Cell 子刊 Cell Host and Microbe 发表研究成果 Arrhythmic Gut Microbiome Signatures Predict Risk of Type 2 Diabetes,作者通过研究 1976 名德国受试者的粪便样本,发现肠道菌群多样性和特定菌群的相对丰度都呈现 24 小时的周期性波动,并确定了影响 2 型糖尿病(T2D)的微生物节律紊乱的 13 个 OTU。此外,通过宏基因组分析能够将 26 种代谢途径与肠道细菌的昼夜振荡联系起来。这些结果表明肠道微生物组昼夜节律与代谢疾病中之间存在功能关联。

图 1 来源:Cell Host and Microbe
2020 年 5 月 27 日,Cell 子刊 Molecular Cell 发表文章 Insulin- and Lipopolysaccharide-Mediated Signaling in Adipose Tissue Macrophages Regulates Postprandial Glycemia through Akt-mTOR Activation,研究表明胰岛素和肠道菌群信号可以协同调控餐后的血糖。我们都知道,免疫细胞在餐后葡萄糖代谢调节中具有十分重要的生理作用。作者发现,进食会升高血清 LPS 和胰岛素,从而在体外诱导巨噬细胞中的 IL-10,而胰岛素和 LPS / 胰岛素处理的巨噬细胞的糖异生基因会被抑制。肥胖症中 IL-10 的产生能力受损,在髓样 IL-10 缺陷小鼠模型中也会出现餐后血糖失调,而肥胖小鼠中表达 IL-10 可以恢复餐后糖异生基因抑制,改善高血糖症状。
关于肠道微生物与肥胖以及糖尿病的关联,从十几年前开始,上海交通大学赵立平教授团队就展开了相关研究,并取得了一系列的成果。2012 年,Science 发表题为 My Microbiome and Me 的 News,介绍了赵立平教授通过两年饮食习惯的改变来调控肠道菌群的事件,他通过高膳食纤维的饮食减重 20 公斤,并且血糖、血压、血脂水平都恢复正常。
通过饮食干预肠道微生物中具有消炎作用的细菌 Faecalibacterium prausnitzii 占据了优势,从其总数的不可检测百分比增加到 14.5%。这种饮食干预方案,一方面把人所需的大量营养素和微量营养素均衡地提供给人体,并且尽可能地增加多样化的膳食纤维,希望能够去改变或者恢复一个健康的肠道菌群结构,进而有可能达到改善肥胖、胰岛素抵抗甚至糖尿病的作用。
 图 2 来源:Science 在此之后,赵立平教授团队一直在肠道菌群领域里面孜孜不倦地探求,2018 年 5 月 9 日,赵教授团队在 Science 发表文章 Gut bacteria selectively promoted by dietary fibers alleviate type 2 diabetes,研究指出,肠道微生物群通过碳水化合物发酵产生的短链脂肪酸(SCFA)对人类有益,而 SCFA 产生的不足与 2 型糖尿病(T2DM)有关。作者专门设计了等能量饮食以及粪便宏基因组学测序进行了一项随机临床研究,以显示膳食纤维促进了一组选择的产生 SCFA 的菌株的繁殖,并且大多数其他潜在的产生菌在 T2DM 患者中有所减少或没有改变。当纤维促进的 SCFA 生产者以更大的多样性和丰度存在时,参与者的血红蛋白 A1c 水平会有更好的改善,部分是通过增加胰高血糖素样肽 - 1 的产生来进行改善的。这些产生 SCFA 的菌株的增加减少了对代谢有害的化合物如吲哚和硫化氢的生产。
图 2 来源:Science 在此之后,赵立平教授团队一直在肠道菌群领域里面孜孜不倦地探求,2018 年 5 月 9 日,赵教授团队在 Science 发表文章 Gut bacteria selectively promoted by dietary fibers alleviate type 2 diabetes,研究指出,肠道微生物群通过碳水化合物发酵产生的短链脂肪酸(SCFA)对人类有益,而 SCFA 产生的不足与 2 型糖尿病(T2DM)有关。作者专门设计了等能量饮食以及粪便宏基因组学测序进行了一项随机临床研究,以显示膳食纤维促进了一组选择的产生 SCFA 的菌株的繁殖,并且大多数其他潜在的产生菌在 T2DM 患者中有所减少或没有改变。当纤维促进的 SCFA 生产者以更大的多样性和丰度存在时,参与者的血红蛋白 A1c 水平会有更好的改善,部分是通过增加胰高血糖素样肽 - 1 的产生来进行改善的。这些产生 SCFA 的菌株的增加减少了对代谢有害的化合物如吲哚和硫化氢的生产。
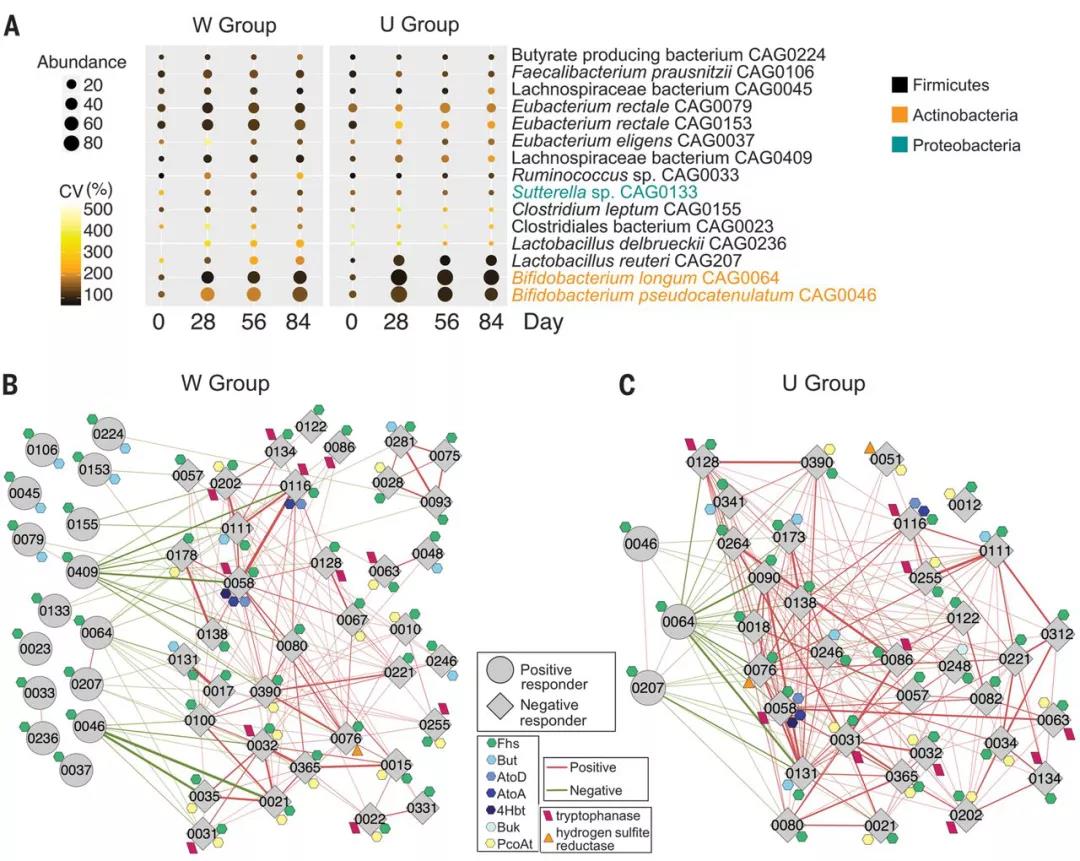
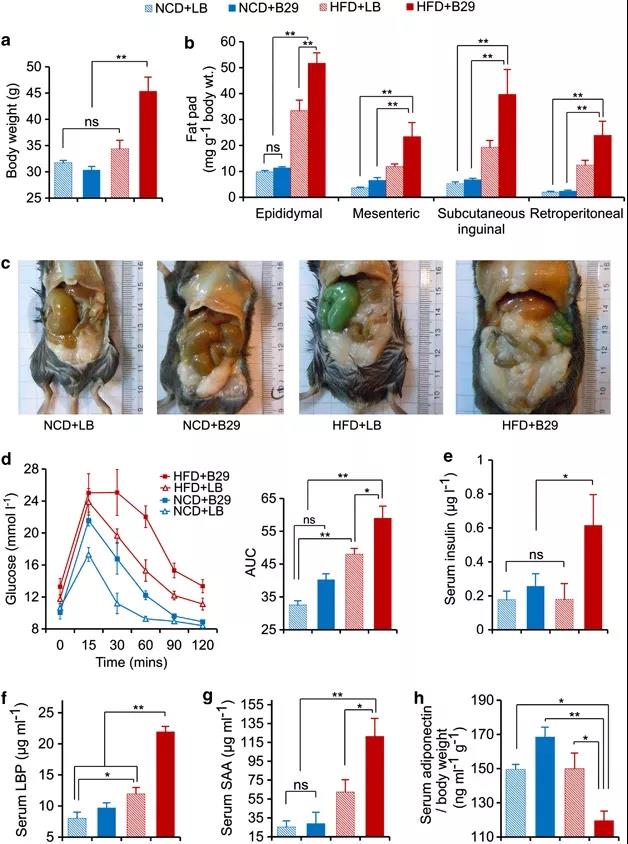
图 3 高纤维饮食有选择地促进了一群 SCFA 生产者成为主要的活跃生产者(来源:Science) 2012 年赵立平团队在 The ISME Journal 上发表研究 An opportunistic pathogen isolated from the gut of an obese human causes obesity in germfree mice,在一个 175 公斤的志愿者的肠道里发现致病菌 Enterobacter cloacae B29,占到了总量的 35%。作者通过给他进行营养干预,食用全谷物、中药食品和益生菌,4 周以后这个菌基本检测不到,23 周以后他的体重下降了 51.4 公斤,并且他的血糖、血压以及血脂全部回到了正常的范围。
无菌 C57BL/6J 小鼠接种了从志愿者肠道分离的 Enterobacter cloacae B29 菌株后在高脂饮食下诱导了肥胖和胰岛素抵抗症状,而在高脂饮食下的无菌对照组小鼠没有表现出相同的疾病表型,Enterobacter cloacae B29 诱导的肥胖小鼠血清内毒素负荷增加,炎症加重。这种人源性内毒素产生物在小鼠中的肥胖诱导能力表明,它可能在其人类宿主中对肥胖的发展起到了致病作用。以上两篇研究都被引用超过 300 次,可见热度之高。
同时,赵教授的研究也给大家提了一些建议,可以多吃多样化的膳食纤维改善我们的肠道菌群。但也并非适合所有人,如果在了解自己的肠道菌群的情况下,更针对性地进行饮食调节会更好。相信在不久的将来,还会有更多的关于肠道菌群与糖尿病的相关研究出现,也会有更多的科技手段可以实现更广泛的测序与研究,或许可以成为一种新的疗法。


你可能喜欢