随着生活水平的提高,肥胖已经成为一种常见的慢性疾病。据统计,仅在我国就已经有超过 3 亿人属于超重和肥胖人群。
机体的过度肥胖除了会诱导多种肥胖并发症比如糖尿病,高血压和心血管类疾病的发生,还会促进肝癌的发展。然而肥胖是否会影响其他类型癌症比如乳腺癌的发生发展目前还不清楚,肥胖是否影响机体的抗肿瘤免疫反应也有待进一步研究。
2019 年 11 月 21 日,来自美国希望之城综合癌症中心的 Hua Yu 教授团队和 Saul Priceman 教授团队合作在 Cell Metabolism 杂志上发表题为《STAT3 Activation-Induced Fatty Acid Oxidation in CD8 + T Effector Cells Is Critical for Obesity-Promoted Breast Tumor Growth》的研究型论文,该论文揭示肥胖诱导 stat3 活化,促进 CD8 +T 细胞氧化磷酸化和乳腺癌发生。

图片来源:Cell Metabolism
主要内容
为了探究肥胖是否影响乳腺癌的发生,作者使用高脂食物饲养能自发乳腺癌的转基因小鼠 PyMT。
结果显示,高脂食物明显诱导 PyMT 小鼠体重增加和肥胖,与此同时,小鼠肿瘤的大小和肺转移也显著增加。这表明肥胖诱导乳腺癌发生。
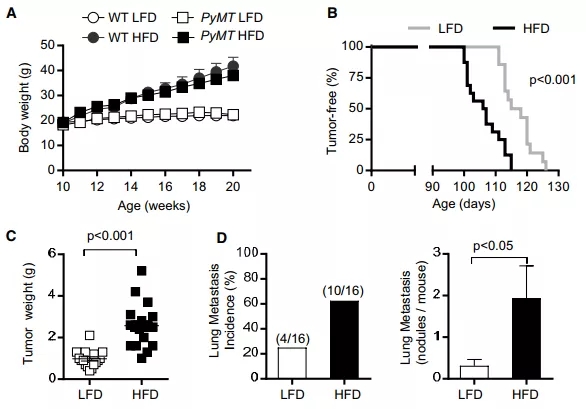
图片来源:Cell Metabolism
接下来作者探究肥胖诱导乳腺癌发生的机制。
CD8 +T 细胞是机体中最重要的抗肿瘤免疫细胞,通过检测肿瘤 CD8 +T 细胞数目和活化情况,作者发现无论是在肥胖的乳腺癌患者还是在肥胖小鼠肿瘤中,CD8 +T 细胞数目明显减少,活化程度也显著降低,这表明肥胖抑制 CD8 +T 细胞功能,从而促进乳腺癌发生。
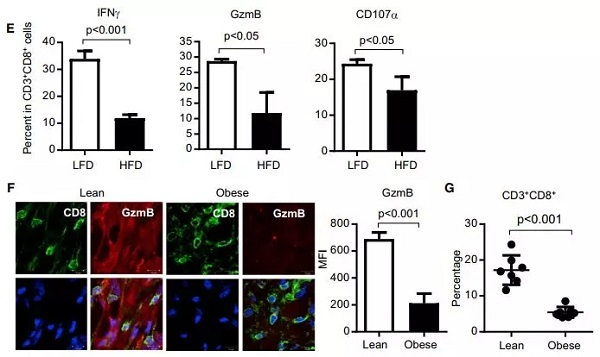
图片来源:Cell Metabolism
肥胖如何抑制 CD8 +T 细胞功能呢?
先前有研究表明,在高脂食物诱导肥胖发生过程中,stat3 的活化至关重要,与此同时,stat3 还是 CD8 +T 细胞活化的抑制因子。因此,作者猜想肥胖通过活化 stat3 来抑制 CD8 +T 细胞功能。
为了验证这个猜想,作者构建了 stat3 的缺陷鼠(stat3 -/-),随后使用高脂食物饲养 stat3 -/-与 PyMT 杂交小鼠,作者发现当 stat3 缺陷后,肿瘤的生长显著降低,CD8 +T 细胞功能明显上调,这表明 stat3 的确能够抑制 CD8 +T 细胞的功能。
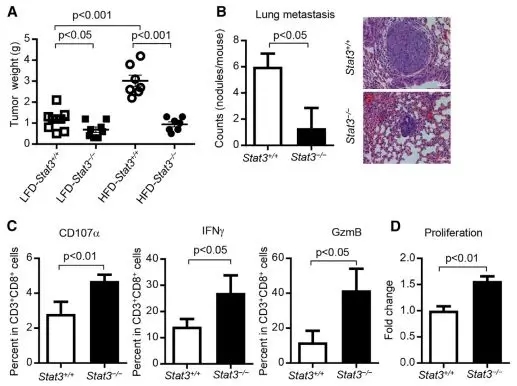
图片来源:Cell Metabolism
接下来作者探究 stat3 抑制 CD8 +T 细胞功能的机制。
越来越多的研究表明 CD8 +T 细胞代谢重编程对其功能的发挥至关重要,在产生 IFN-γ过程中,CD8 +T 细胞更趋向于糖酵解代谢途径。
通过检测 CD8 +T 细胞中糖酵解过程关键酶的表达和氧化呼吸率,作者发现当 stat3 缺陷后,CD8 +T 细胞中糖酵解过程上调,氧化磷酸化途径被抑制,这表明 stat3 通过诱导 CD8 +T 细胞氧化磷酸化来抑制后者的功能。
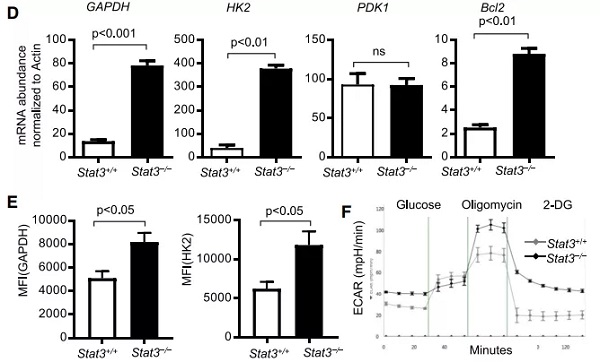
图片来源:Cell Metabolism
下游的分子机制已经研究清楚,接下来作者探究肥胖如何诱导 stat3 活化。
肥胖最主要的外在特征就是脂肪细胞堆积,后者能够分泌瘦素抑制脂肪细胞的合成,避免机体过度肥胖。
肥胖诱导 stat3 活化是否依赖于瘦素呢?
使用抗体中和瘦素后,作者发现 stat3 的活化受到明显抑制,CD8 +T 细胞糖酵解途径和功能显著增强。
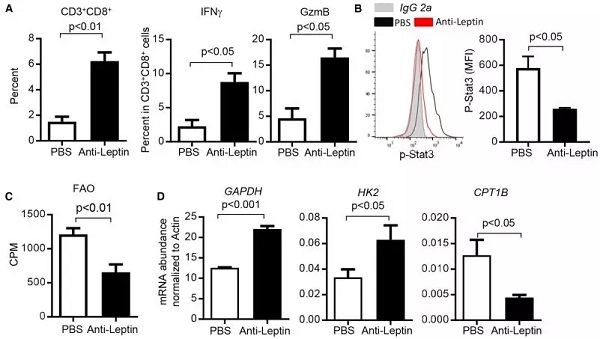
图片来源:Cell Metabolism
前期研究
其实,这并不是 Hua Yu 教授团队第一次揭示代谢与癌症的关系。
2018 年 1 月 9 日,他和他的团队在 Cell Metabolism 杂志上发表题为《JAK/STAT3 -Regulated Fatty Acid b-Oxidation Is Critical for Breast Cancer Stem Cell Self-Renewal and Chemoresistance》的研究型论文,该论文揭示 JAK/STAT3 信号通路调控的脂肪酸 β 氧化对于乳腺癌干细胞的自我更新和化疗抵抗至关重要。

图片来源:Cell Metabolism
2018 年 11 月 15 日,来自澳大利亚莫纳什大学的 Tony Tiganis 教授团队在 Cell 杂志上发表题为《Obesity Drives STAT- 1 -Dependent NASH and STAT- 3 -Dependent HCC》的研究型论文,该论文揭示肥胖不仅能够通过 stat1 促进非酒精性脂肪肝发生,还能诱导 stat3 活化促进肝癌的发生。

图片来源:Cell
小结
总结这篇文章,作者发现肥胖病人和小鼠中大量堆积的脂肪细胞产生瘦素,后者激活 stat3,促进 CD8 +T 细胞氧化磷酸,抑制 CD8 +T 细胞功能和抗肿瘤免疫,从而促进乳腺癌的发生。
该论文不仅揭示了肥胖促进乳腺癌发生的机制,还为乳腺癌的治疗提供新的思路,可以通过阻断瘦素或者逆转 CD8 +T 细胞氧化磷酸化来治疗乳腺癌。

图片来源:Cell Metabolism
总之,肥胖与人类多种癌症的发生发展密切相关。该论文揭示了肥胖促进乳腺癌发生的具体机制,为乳腺癌的代谢疗法提供新的证据,希望不久的将来,我们能看到代谢疗法在乳腺癌治疗中发挥着至关重要的作用。


你可能喜欢