由于与机体发育、器官大小调控、组织稳态和肿瘤发生密切相关,近些年来,关于 Hippo 信号通路的研究也越来越受到重视。
先前的研究表明,Hippo 信号通路实质上是一个激酶级联反应介导的生长抑制信号通路。
在感知多种信号刺激时,比如细胞连接、细胞极化、血清饥饿和溶血磷脂酸(LPA)缺乏,Hippo 信号通路中的关键激酶 MST1 / 2 和 MAP4Ks 会磷酸化活化 LATS1 / 2 激酶,后者诱导 YAP/TAZ 磷酸化,抑制 YAP/TAZ 入核启动靶标基因表达,从而阻断 YAP 的促生长,抗凋亡等功能。
0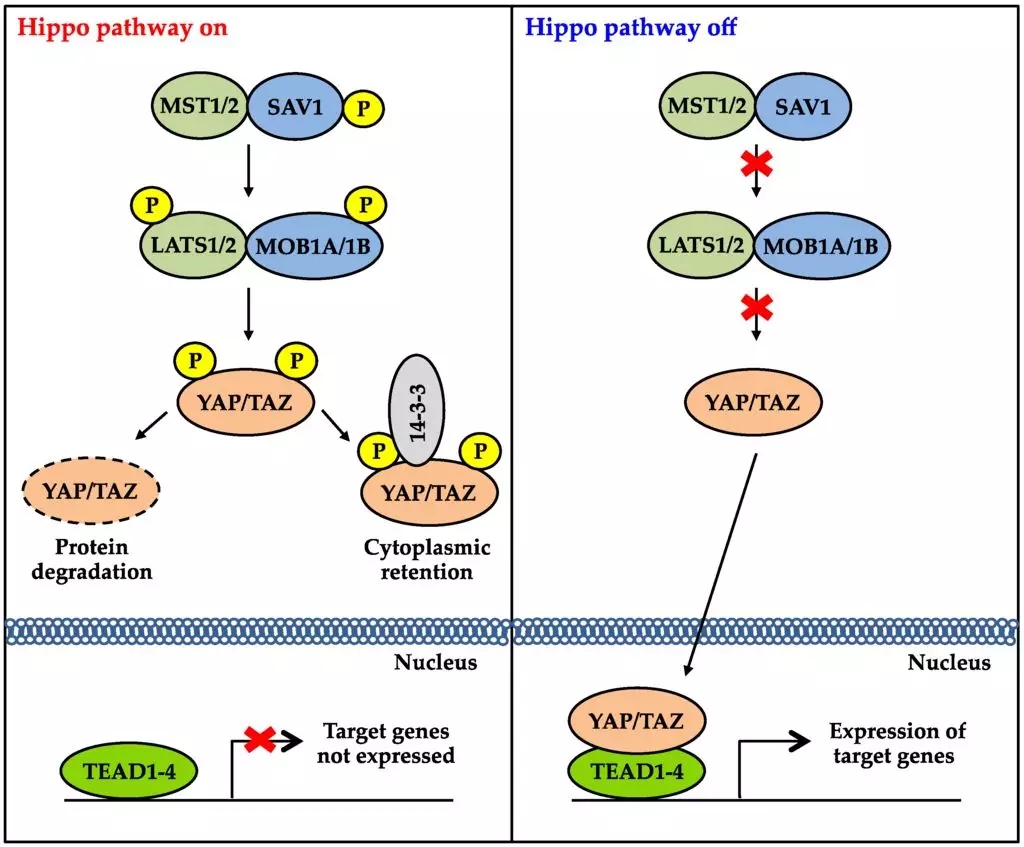
图片来源:google
虽然目前的研究已经表明 MST1 / 2 和 MAP4Ks 是 Hippo 信号通路上游关键激酶,但是外界多种信号如何促进 MST1 / 2 和 MAP4Ks 的活化目前还不清楚。
2019 年 12 月 2 日,来自加州大学圣地亚哥分校管坤良团队在 Nature Cell biology 杂志上发表题为《STRIPAK integrates upstream signals to initiate the Hippo kinase cascade》的研究型论文,该论文发现 STRIPAK 能够调控 Hippo 信号通路活化,从而促进肿瘤发生。

图片来源:Nature cell biology
主要内容
STRIPAK 是细胞中与肿瘤发生密切相关的重要蛋白复合物,由典型的 PP2AC 催化亚基、STRN 相互作用蛋白(STRIP1 / 2)和膜相关蛋白 SLMAP 组成,也能够与 MST1 和 MAP4K4 结合。
先前有文章指出,细胞中表达的 STRIPAK 能够与 Hippo 信号通路中激酶相互作用,从而阻断 Hippo 信号通路活化。因此,作者猜想血清饥饿等信号是否能影响 PP2A 和 Hippo 激酶结合。
通过免疫共沉淀实验,作者发现当加入血清或者 LPA 后,PP2A 的催化 C 亚基 PP2AC 与 MST1 和 MAP4K4 相互作用显著增强。
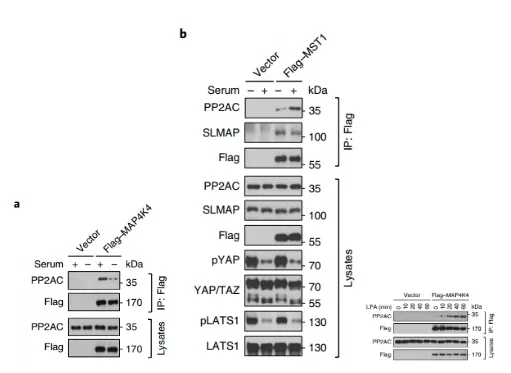
图片来源:Nature cell biology
那么 STRIPAK 复合物中其他结构蛋白是否也参与 Hippo 信号通路活化?
细胞中敲除 STRIP1 / 2 和 SLMAP 后,作者发现 LPA 或者血清对 Hippo 信号通路的抑制作用得到缓解。这表明 STRIPAK 对 LPA 或者血清抑制 Hippo 信号通路至关重要。
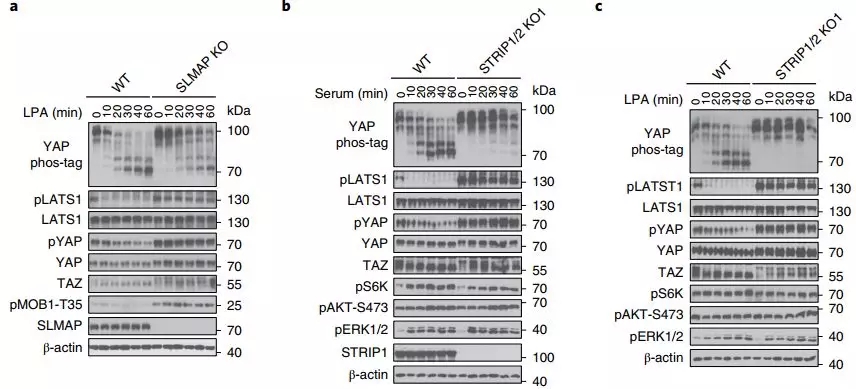
图片来源:Nature cell biology
接下来作者探究其中的具体机制。
先前有研究表明 LPA 调控 Hippo 信号依赖于 RhoA,那么 RhoA 在 MAP4K4 和 STRIPAK 相互作用中是否扮演角色?
使用 RhoA 失活诱导剂肉毒杆菌毒素 C3 处理细胞或者转染 RhoA 失活突变体 RhoA N19 质粒,作者发现 LPA 诱导的 MAP4K4 和 STRIPAK 相互作用受到明显抑制。
这表明 LPA 通过 RhoA 促进 MAP4K4 和 STRIPAK 结合。
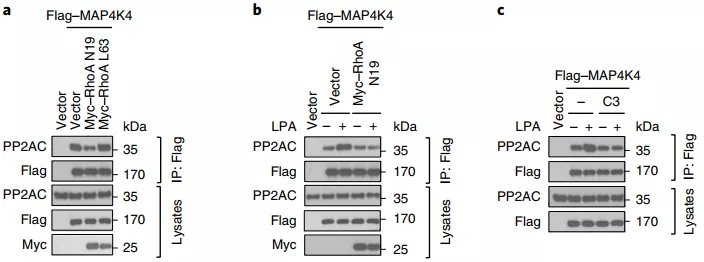
图片来源:Nature cell biology
既然 RhoA 对 MAP4K4 和 STRIPAK 的结合有促进作用,那么这种调控作用的机制是什么?
在 Hippo 信号通路活化过程中,Kibra(WWC1)和 NF2 是位于 RhoA 下游另外两个重要的 Hippo 信号调控蛋白。
通过免疫共沉淀实验,作者发现当过表达 Kibra 和 NF2 时,MAP4K4 和 STRIPAK 相互作用显著下降。
与此同时,敲低 Kibra 或 NF2 能够明显恢复 RhoA 失活突变体 RhoA N19 对 MAP4K4 和 STRIPAK 相互作用的抑制作用。这表明 RhoA 通过下游的 Kibra 和 NF2 抑制 MAP4K4 和 STRIPAK 相互作用。
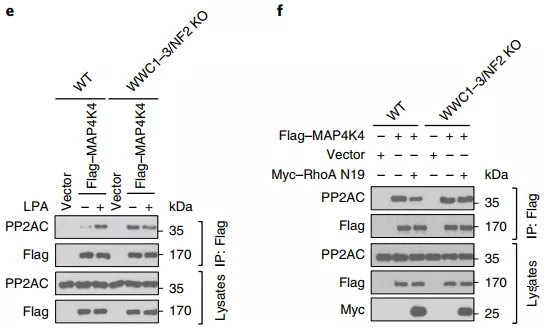
图片来源:Nature cell biology
作者通过生物信息学网站 bioplex 进行预测,发现 RHPN 可能与 Kibra 相互作用。随后通过实验进行验证 RHPN 和 Kibra 的确存在相互作用,并且它们相互作用受到 RhoA 调控,随后促进 Hippo 信号通路活化。
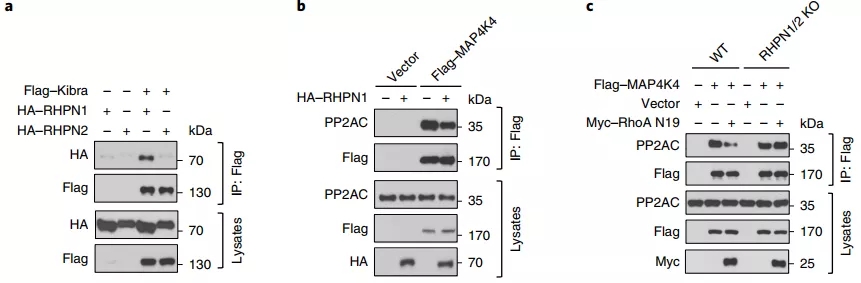
图片来源:Nature cell biology
先前的研究表明 Hippo 信号抑制肿瘤细胞生长,既然 RHPN 能促进 Hippo 信号通路活化,那它是否也能抑制肿瘤细胞的生长?
通过对人结肠癌细胞系 HCT116 细胞进行观察,作者发现过表达 RHPN 后,细胞增殖能力显著降低;但是敲低 LATS 后,细胞的增殖能力提高。这表明 RHPN 通过 Hippo 信号通路抑制肿瘤发生。
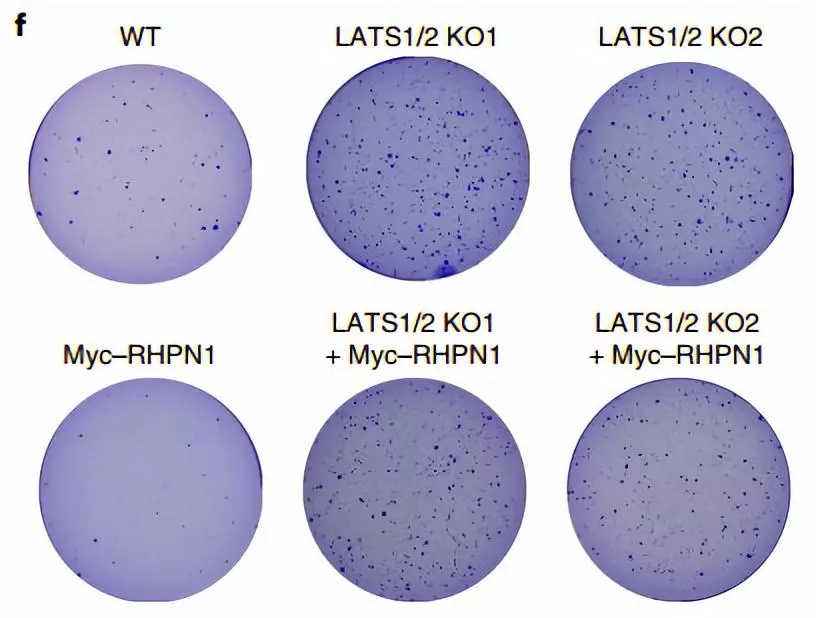
图片来源:Nature cell biology
前期研究
其实,这并不是管坤良教授团队第一次研究 Hippo 信号通路的活化机制。2018 年 8 月 22 日,他和他的团队在 Nature 杂志上发表题为《RAP2 mediates mechanoresponses of the Hippo pathway》的研究型论文,该论文揭示 RAP2 能够感知机械应激压力,从而活化 Hippo 信号通路。

图片来源:Nature
2017 年 7 月 28 日,同样是来自于管坤良教授团队在 Nature cell biology 杂志上发表题为《Regulation of Hippo pathway transcription factor TEAD by p38 MAPK-induced cytoplasmic translocation》的研究型论文,该论文揭示 p38 MAPK 信号能够诱导 Hippo 信号通路下游转录因子 TEAD 向细胞质中转运,从而抑制 Hippo 信号通路活化。

图片来源:Nature cell biology
2016 年 12 月 1 日,管坤良教授团队在 Cell 杂志上发表题为《The Hippo Pathway Kinases LATS1 / 2 Suppress Cancer Immunity》的研究型论文,该论文揭示 Hippo 信号通路中的关键激酶 LATS 能够抑制机体抗肿瘤免疫。

图片来源:cell
可以看到,华人管坤良教授在 Hippo 信号通路活化调控及相关疾病治疗中做出了巨大贡献。
小结
总结这篇文章,作者发现血清饥饿或者 LPA 缺乏诱导 Hippo 信号通路活化,抑制肿瘤发生的具体机制:
血清饥饿或者 LPA 缺乏时,RhoA 功能受到抑制,接着抑制 RHPN 和 Kibra/NF2 形成复合体,随后进一步抑制 STRIPAK 与 MST1 / 2 和 MAP4Ks 相互作用,因此激活了 Hippo 信号通路,诱导 LATS 和 YAP 发生磷酸化,导致 YAP 无法入核启动靶标基因转录表达。
该论文不仅揭示了 Hippo 信号通路活化的机制,还发现 RHPN 具有肿瘤抑制子功能,能够抑制肿瘤发生,为肿瘤治疗提供新的靶点。
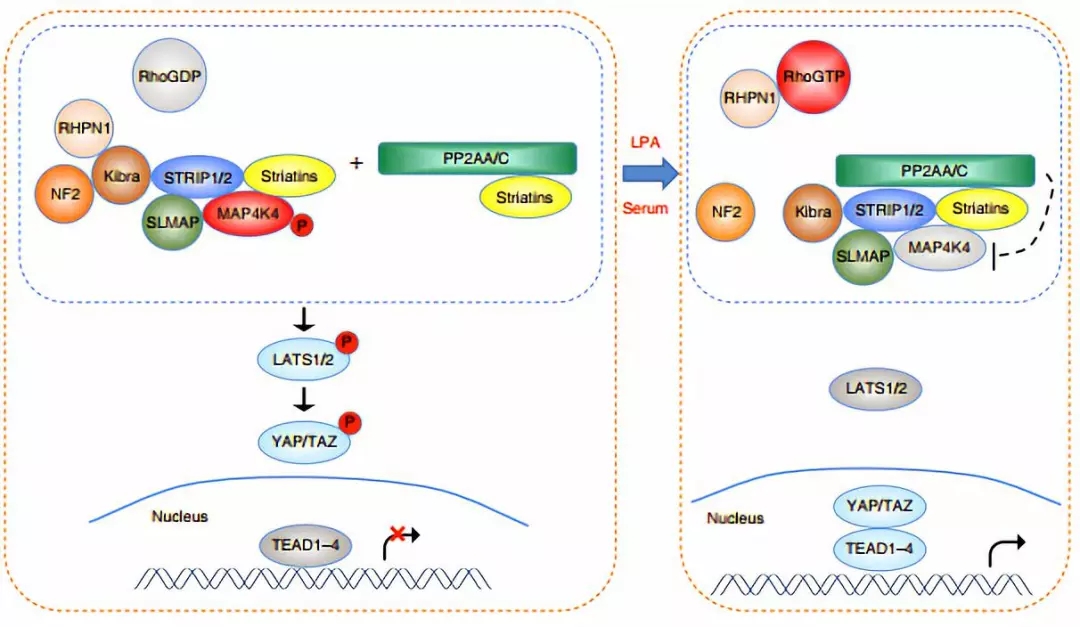
图片来源:Nature cell biology
最后笔者也希望靶向 Hippo 信号通路的抗肿瘤药物能尽快面世,为肿瘤提供新的治疗方法。


你可能喜欢